■ 前言:推甄必看!研究所考前猜題補帖
每年十月,科研人員最關注的莫過於諾貝爾獎得主的揭曉。這不僅是學界的最高榮耀,更是碩博班導師最愛抽考、推甄面試必備的加分題。若能在面試時對當屆得主的研究侃侃而談,幾乎等於一隻腳踏進了研究所大門。
今年(2023)的諾貝爾生理學或醫學獎,由 卡里科(Karikó Katalin) 與 魏斯曼(Drew Weissman) 這對合作超過 25 年的老搭檔共同獲得,將平分1100 萬瑞典克朗(約100 萬美元)。這場獲獎幾乎毫無懸念,因為他們在 2021 年就已橫掃醫學界僅次於諾貝爾獎的「拉斯克獎」與「霍維茨獎」。因此,可以看出這兩位科學家在學界享有極高的聲望,只要他們保持健康活得夠長,摘下桂冠只是遲早的事(諾貝爾僅頒給在討論年度獲獎者當下活著的人)。
獨佔諾貝爾經濟學獎的第一人,「女性經濟學」Claudia Goldin

2023年諾貝爾醫學獎兩位得獎人Karikó Katalin與Drew Weissman
當然,臺灣企業家尹衍樑創立的唐獎,在2022年也成功預測,不過他們同時帶上了Pieter Cullis這位脂質奈米顆粒(Lipid nanoparticles)的先鋒者。我個人是覺得蠻合理,畢竟三要件缺一不可,不過諾貝爾家頒獎的習慣是要長期合作,才會被視為一個計畫的共同發起人,所以沒有算上 Pieter Cullis 也在情理中。
老慣例,我會說明研究內容,但當然因為這是醫學獎會比之前經濟學獎涉及更多專業知識,我盡量在白話與保持文章專業性中平衡。
■ 研究重點:mRNA 疫苗的「解碼」關鍵
這項研究之所以成為大熱門,關鍵在於:如何讓外來的 mRNA 順利進入人體,而不引發致命的免疫攻擊?
1. 關鍵突破:核苷修飾技術
在 Karikó 與 Weissman 突破困境前,體外轉錄的 mRNA 進入人體後,會被類鐸受體(TLRs)辨識為外來入侵者,引發劇烈的發炎反應。
- 發現契機:他們觀察到實驗中的 tRNA 不會引起強烈免疫反應,進而得出見解:經過特定核苷修飾(如以「假尿苷」替換「尿苷」)的 RNA,可以大幅降低免疫反應。
- 運作機制: mRNA 能順利進入細胞,指示人體製造新冠病毒的「刺突蛋白(Spike protein)」,讓免疫系統進行模擬演習,產生記憶與保護力。
2. 完美的平台:脂質奈米顆粒 (LNP)
雖然諾貝爾獎頒給了 Karikó 與 Weissman,但不可忽視的是 Pieter Cullis 在脂質奈米顆粒技術上的貢獻。正是因為 LNP 的包覆技術,修飾過的 mRNA 才能被安全送達細胞。這是一個三位一體、缺一不可的完整載體平台。
新型疫苗會成為大熱門的關鍵在於,如何產生免疫細胞,製造疫苗抗原,用以對抗新型冠狀病毒(COVID-19)。如果沒有他們所開發出的修飾技術,能順利進入人體,讓細胞製造新冠病毒表面的刺突蛋白/棘蛋白記憶此類病毒蛋白。
這種技術讓人體能夠應對不斷變化的病毒,因為透過mRNA製造病毒的特殊「標誌」(Mark),允許我們的免疫系統進行模擬演習。在實際面對病毒時,我們的免疫系統就能發揮作用,進而降低死亡率和重病率。
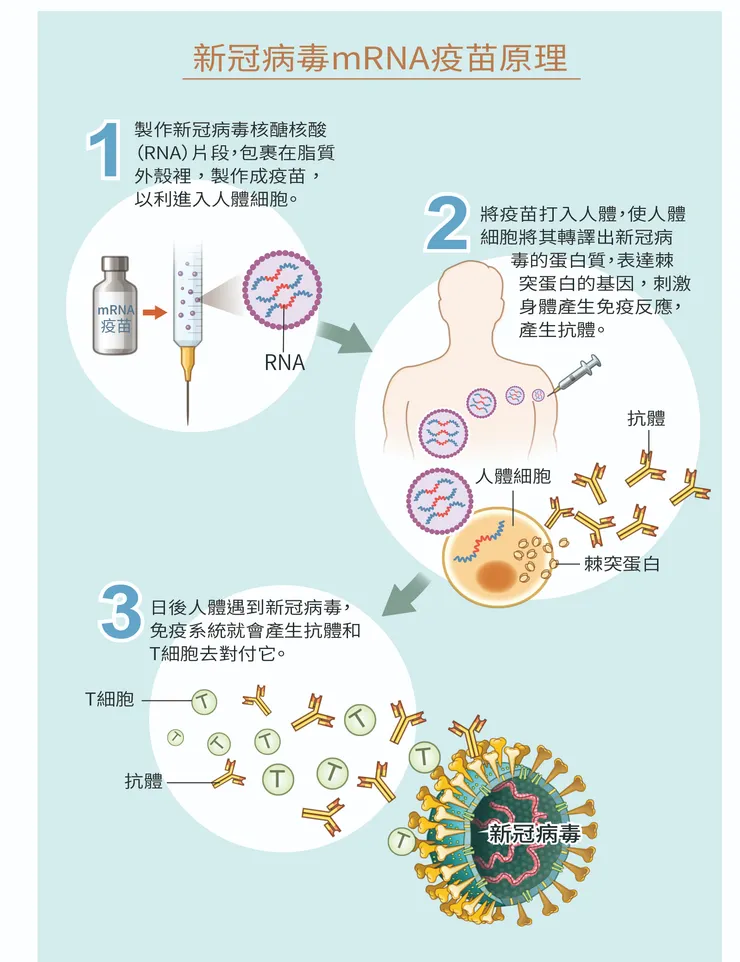
圖源: 財團法人全民健康基金會
■ 為何稱為「最速傳說」?
因為他們在研究中突破了當時的困境,並將這一突破迅速應用於實際醫學治療中。傳統藥物從開發到上市通常需要 15 至 20 年,但 mRNA 技術從 2013 年臨床實驗、2019 年爆發疫情,到迅速投入全球防疫,在醫學史上簡直是奇蹟。這背後並非僥倖,而是 Karikó 數十年的堅持——她曾因為這項「沒人看好」的研究被要求轉換方向,甚至遭到降職。
這項技術的潛力不僅止於 COVID-19,未來更可用於:
- 癌症免疫療法:教導免疫細胞辨識癌細胞表面蛋白。
- 多能幹細胞生成:對再生醫學產生重大影響。
背景說明
Drew Weissman 早期是名醫生並以免疫學和微生物學方面的論文為主要創作,直到遇上Katalin時才開始嘗試將 RNA 和先天免疫系統生物學結合。
而 Katalin 早期研究的重點其實偏向生物化學,在研究分類上偏向基礎研究的細胞信號傳送蛋白干擾素(Interferon, IFNs)研究。但因為博士後期間接觸過雙股 RNA (dsRNA) 於臨床上的治療,使她著手於攻克信使 RNA (mRNA)進入人體後產生的劇烈免疫反應。這是由於mRNA會被類鐸受體(Toll-like receptors, TLRs)辨識,使先天性免疫細胞反應,導致生物產生嚴重的發炎反應。
許多人都相信,只要能抑制下相關免疫反應,mRNA將成為最好的載體,但是沒有人有辦法攻克,乃至於許多研究人員、生物技術和製藥公司對其潛力表示懷疑。Katalin也從有望成為教授的新星,被要求轉換研究方向,甚至降職,但她仍然堅守著信念,也在此時她與Weissman相遇。
後續他們觀察到實驗中用作對照的轉移 RNA (Transfer RNA,tRNA)不會引起與 mRNA 相同的免疫反應時,得出了一個重要的見解,經過特定核苷修飾的RNA可以大幅降低免疫反應。(假尿苷替換尿苷)。
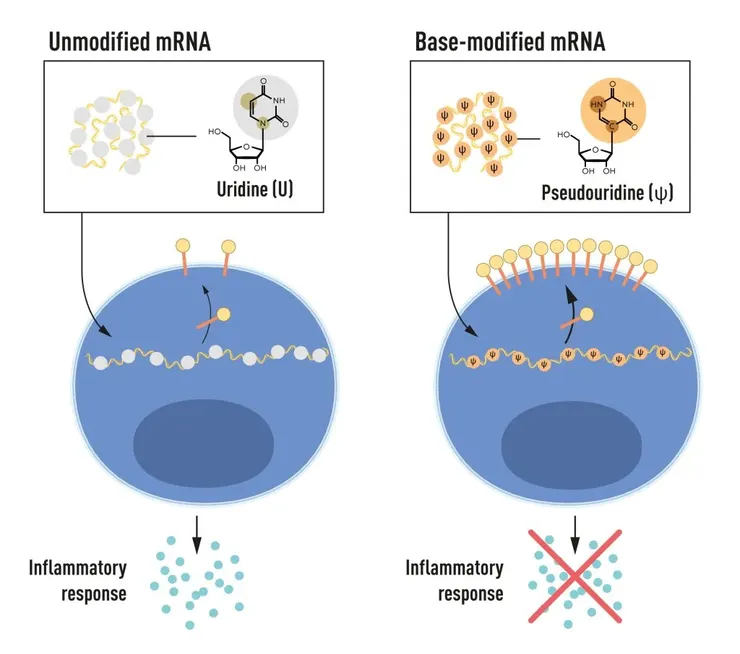
經過特定核苷修飾的RNA可以大幅降低免疫反應
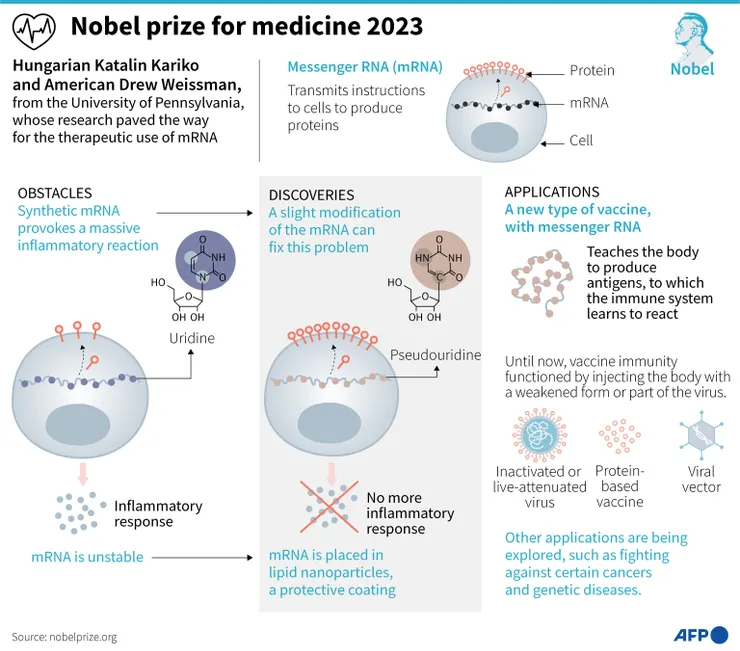
Nobel Prize For Medicine 2023
Karikó 和 Weissman 創立了一家小公司 RNARx,並於 2006 年和 2013 年獲得了使用幾種修飾核苷的方法,來減少針對 mRNA 的抗病毒免疫反應的專利。
並由 Pieter Cullis 的脂質奈米顆粒包覆,送入人體,形成一個完整的載體平台。
從1997年發現特定核苷修飾至2013年他們就完成了臨床實驗並投入生產,最終在2019年發會關鍵作用廣泛投入實際應用,這在整個醫療開發界不可不謂之是奇蹟。
傳統上光一個小分子藥要走向銷售都要 15~20 年,更何況這種有對人體基因進行改造可能的行為。當然 COVID-19 的迫切需求也加速了這個過程,但如果沒有事先進行充分的準備,即使風起時,也難以高效地推動這一技術的應用。
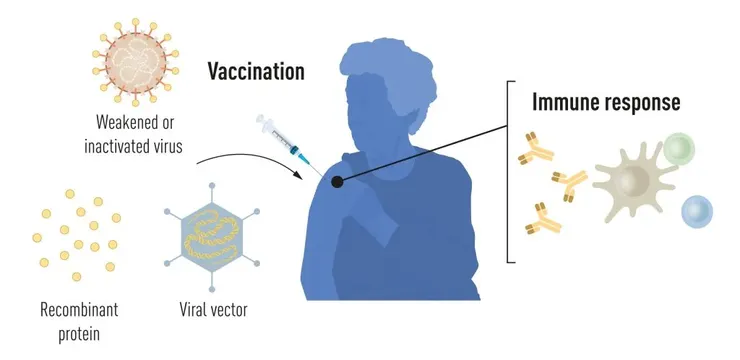
不同種類的疫苗製作方式
■ 個人觀點:除了 mRNA,我們還有其他選擇嗎?
雖然 mRNA 是當紅炸子雞,但人類對抗病毒是多線並進的。目前主流還有三種技術:
(1)蛋白質次單元疫苗
此一技術通過基因重組,直接製造出病毒表面的棘狀蛋白,以作為疫苗注射入人體,從而引發免疫反應。
(2)病毒載體疫苗–線病毒疫苗
將製造病毒表面棘狀蛋白的DNA片段放入無害的腺病毒中,然後遞送至人體細胞,以誘發免疫反應。
(3)全病毒疫苗
將病毒用打碎或高溫等滅活性,降低其傳染性再打入人體。
值得注意的是,每種疫苗技術都具有一定程度的保護效果,儘管採用滅活病毒的方法相對不太可控,因此其保護效力相對較低。但它們在製作成本和生產效率方面相對經濟實惠,因此目前仍然是一種選擇。因為存在這些方法,我們不應誇大 Karikó Katalin 和 Drew Weissman 的作用,將他們視為救世主。然而,無可否認的是,他們的研究推動了整個人類醫學研究的進程。
■ 結語:基礎研究是學術的根本,也是人才的淬煉
我自己在大學到研究所的過程中,從化學藥品的合成開發轉往生物的轉譯後修飾,最常被問到的問題就是:
你研究這個有什麼用處?能有什麼醫療貢獻?
(化學合成一般都是對重要藥品的成品率、反應時間或對官能基修飾優化,以實際應用為目的,所以這個問題相對容易回答)
我個人蠻贊同導師的一句話:
「基礎研究是學術的根本,是人才培育的過程。」
如果我們沒有弄清楚整個生理結構的機轉,去期待發現什麼能直接應用於臨床的技術,其實就跟買樂透企圖一獲千金都是在跟未知賭,也無法預測是否會帶來嚴重的後果。
關於目前過分執著於模仿天然化合物的問題,在 2022 年的諾貝爾化學獎功能化學獲獎時也有被提出,這個未來有機會再展開說。
雖然我後來最終任職於 API 藥廠,又走回化學合成為主,甚至走向與研究無關的Sourcer。但這樣的系統性學習,也養成了我整理資料的習慣。
在前期學術累積的過程必然緩慢且乏味,但當準備充足時,不論走到哪裡,都會有你的舞台。唯有曾經留下的汗水不會背叛。就像當年的我預測到自己可能會以撰寫文章與預測趨勢維生,卻沒有想到是以這樣的形式,每當入秋就關注著諾貝爾獎的頒發,也成為了一種習慣。
執著於熱情所在,才能發出最耀眼的光芒。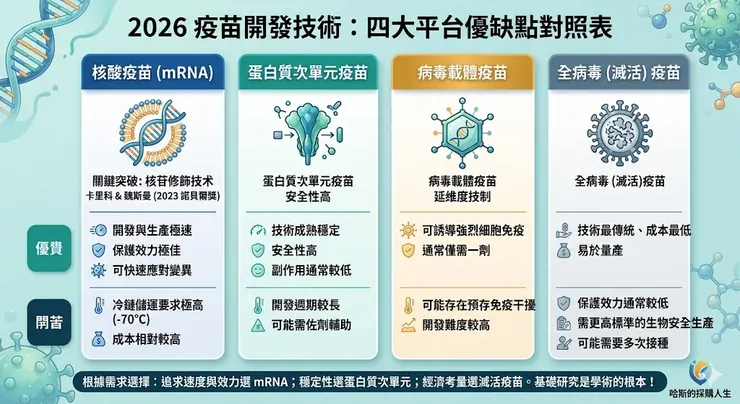
■ 參考文獻:
1.https://www.twhealth.org.tw/journalView.php?cat=56&sid=954&page=1
2.https://www.nobelprize.org/prizes/medicine/2023/press-release/
3.https://www.tang-prize.org/owner_detail.php?cat=11&id=2036
4.https://www.cgmh.org.tw/cgmn/category.asp?id_seq=2103011
5. https://pansci.asia/archives/119670

我是哈斯的採購人生, vocus 主題專家野格團,專門負責閱讀與理財相關💰
感謝您閱讀本篇文章。
❤️ 喜歡本篇文章請幫我按【愛心】
✅ 持續來點靈感歡迎按下【追蹤】
🧋 敲碗指定報導請選【贊助珍奶】





