在前兩篇文章中,我們從 RA(法規事務)的視角,透視了入行必備的「六大基本功」,並晉升為「戰略指揮官」,佈局全球註冊策略。我們談論了如何在理性的框架下,勾勒產品通關的嚮導。
然而,在醫藥這個「以生命為本」的行業裡,光有地圖與策略是不夠的。你要如何證明你的地圖是真實的?你要如何保證你的策略背後,每一筆數據、每一個實驗、每一顆藥丸,都是誠實且可信的?
這就引出了醫藥產業的「誠信憲法」:GxP (Good x Practice)。
-------------------------------------------------------------------------------------------------------
職人閱讀指南與聲明: 本文內容係基於筆者在**藥品(Medicinal Products)與生物製品(Biological Products)監管領域之個人實務經驗與觀察彙整而成。若讀者從事醫療器材(Medical Device)等其他產業,其具體引據法規(如 ISO 13485 等)與本文論述之藥品體系有所區別。
同時,本文觀點僅供專業交流與實務參考,不代表任何官方主管機關之立場或最終解釋。法規實務存在個案差異,具體執行請務必參閱各國現行公告之正式條文。
-----------------------------------------------------------------------------------------------------------------------------
如果說 RA 是在監管機關面前為產品「辯護」的律師,那麼 GxP 就是那套「不可抹滅的證據法則」。它不是單一的法規,而是一系列「優良操作規範」的總稱,涵蓋了藥品從研發、臨床、製造到最終運銷的全生命週期。
很多行外人(甚至部分業內人)覺得 GxP 只是繁瑣的文件堆疊,是限制創新的絆腳石。但在專業 RA 眼中,GxP 是醫藥產業最核心的「信任合約」:它確保了數據的真實,從而守護了患者的安全。
今天,我們就用理性的濾鏡,解密醫藥產業 GxP 家族裡最大的五大核心成員:GLP、GCP、GMP、GDP 與 GTP。
GxP 家族大解密:五大誠信支柱
GxP 中的「x」代表不同的領域,但「Good Practice」的核心始終如一:數據必須真實、流程必須可控、結果必須可重現。為了讓你快速建立直覺,我製作了這張對照表:
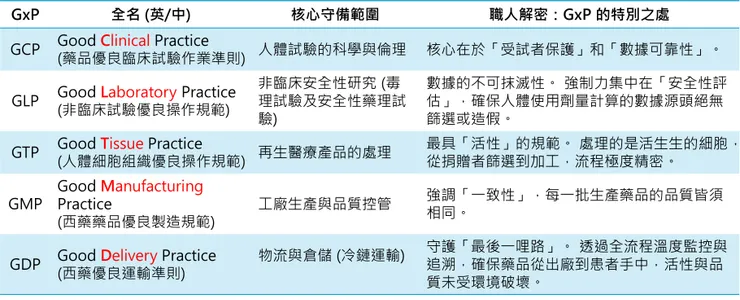
一、 GLP (Good Laboratory Practice):數據的原始「初戀」
在實務操作中,藥廠會進行大量的「藥效評估(Efficacy)」或「機制探索」,這些探索性試驗通常不強制要求 GLP 認證。GLP 的強制力主要作用於「毒理試驗(Toxicology)」與「安全性藥理試驗(Safety Pharmacology)」。因為這些試驗的結果直接決定了人體受試者的初始風險評估(如計算首次使用於人體 "First-in-Human" 劑量),監管機關要求其必須在具備 GLP 認證的實驗室中,按照嚴格的品質體系執行。
在 RA 眼中,GLP 的特別之處在於它對「數據原始性」的執著。GLP 要求所有實驗數據必須真實記錄,且不可抹滅。這意味著,如果你在實驗中打翻了試管、如果不小心操作錯誤導致動物死亡,你不能把這筆數據刪除,假裝沒發生過。你必須如實記錄這個失敗,並解釋原因。
為什麼?因為監管機關要確認,你最終提交的「完美數據」,不是從一堆失敗數據中「篩選」出來的。GLP 證明了數據的起點是誠實的。
二、 GCP (Good Clinical Practice):生命與倫理的黃金天平
當藥品準備進入人體(臨床試驗)時,GCP 就正式接管了戰場。這是 GxP 家族中倫理色彩最濃厚、法規要求最細膩的一員。
在 GCP 的世界裡,運作的核心圍繞著三個關鍵角色:試驗委託者 (Sponsor)、試驗主持人 (PI) 與受試者 (Subject)。而維繫這三者關係的靈魂,則是「受試者同意書 (ICF)」與「人體試驗委員會 (IRB/EC)」。
GCP 的核心不是「證明藥有效」,而是「受試者保護」與「數據可靠性」。在 GCP 的邏輯裡,如果為了證明藥物有效而犧牲了受試者的安全或隱私,這份數據在法律與道義上都是「無效」的。
在 RA 的視角裡,GCP 是一場極其嚴謹的「程序正義」。一個數據造假的 GCP 報告,不僅會終結產品的研發,甚至會引發法律風暴。GCP 證明了數據的獲取,是在最高倫理標準與嚴謹科學設計下完成的。
三、 GMP (Good Manufacturing Practice):工廠裡的「一致性」魔術
在實務中,GMP 並非從研發第一天就火力全開。在早期的臨床試驗階段(Phase I/II),由於製程尚在優化且臨床用藥量小,法規通常要求的是符合 「GMP 的精神(In the spirit of GMP)」,即確保基本的安全性、追溯性與不交叉污染,而非要求完全比照上市藥品的嚴苛標準,這也是基於研發成本與彈性的合理權衡。
然而,隨著研發進入 Pivotal Trial(關鍵臨床試驗/三期臨床),情況會發生質變。為了確保臨床數據的代表性,並為未來的上市申請(NDA/BLA)做準備,專業藥廠通常在執行 Pivotal Trial 之前,就會要求製程與廠房自行達到完全符合 GMP 的標準(Full GMP Compliance)。因為如果關鍵試驗所用的藥物與未來上市的藥物在品質上有顯著差異,將可能導致臨床數據無法被監管機關認可,甚至必須重新補做試驗。
一般的 RA 追求「核准」,而 GMP RA 追求的是「一致性」。GMP 要證明,你在實驗室裡做出的那顆「完美藥丸」,在工廠大規模生產時,第 1 顆、第 10,000 顆、甚至第 1,000,000 顆,它們的純度、濃度與活性,都必須像同卵雙胞胎一樣精準、一致。
四、 GDP (Good Distribution Practice):冷鏈運輸的「最後一哩路」
藥做好了,要怎麼安全地送到醫院、藥局,甚至患者手中?這就是 GDP 的戰場。它守護的是「物流與倉儲」。
GDP 看似簡單,實則處處玄機,特別是對「冷鏈運輸」的偏執。以疫苗為例,如果在運輸過程中溫度波動超過了規定的範圍,疫苗的活性就會失效。藥廠和病人都不希望辛苦做出來的藥品,因為最後運輸過程中的瑕疵,而毀於一旦。因此,GDP 要求全流程的溫度追溯,證明藥品從出廠到交付,始終維持在最佳狀態。GDP 證明了數據的完整性,在最後一哩路沒有崩塌。
五、 GTP (Good Tissue Practice):最具「活性」的新興規範
最後,我們來到醫藥界的最前沿:再生醫療,這裡是 GTP 的領地。
(在台灣,再生醫療指的是用基因、細胞及其衍生物,用以治療、修復或替換人體細胞、組織及器官之製劑或技術。)
很多人會混淆 GTP 與 GMP,認為兩者只是細緻程度的差別,實則不然。兩者的「精神」有本質上的不同:
- GMP 的核心是「一致性」: 確保每一批藥物的品質、純度、含量都如同工廠模具刻出來般精準。
- GTP 的核心是「防止疾病傳播」: 由於細胞與基因治療產品(如骨髓、幹細胞、免疫細胞)具有高度的「活性」與「異質性」,很難像化學藥物那樣要求絕對的一致,而且這類再醫療藥物製作完成後,不能像一般的藥物一樣直接進行滅菌。因此,GTP 的重中之重在於防範傳染病發生的風險。從細胞捐贈者(Donor)的篩選、採集、處理到最終植入,都要確保這套「活的藥物」在過程中不會造成病毒、細菌或其他病原體的交叉污染與傳播。
值得一提的是,GTP 是台灣法規環境下的一個特色產物。為了因應細胞治療的蓬勃發展,台灣衛生福利部採用了民國 91 年所制定的「人體細胞組織優良操作規範」,作為醫療機構與生物技術業者在處理人體細胞組織時的最高準則 (雖然我覺得這法規已經過時)。因此,在台灣,如果想要申請執行再生醫療製劑的臨床試驗,除了試驗計畫書須經食藥署審核通過外,生產試驗藥品的工廠,以及執行臨床試驗的每一家醫療院所,都必須經食藥署人員至現場稽查 (稱為GTP 訪查) 通通過後,才可以執行,這應該是全世界獨有的程序。針對台灣 GTP 訪查的程序和眉角,可以另開一篇專文來介紹。
【結語:從「數據」到「信任」的ALCOA+魔法】
介紹完 GxP 家族成員,你可能會問:它們有沒有一個共同的靈魂?有的,那就是「ALCOA+」原則。簡單來說,GxP 要求數據必須是:
- Attributable (可追溯:誰做的?)
- Legible (清晰:看得懂嗎?)
- Contemporaneous (同步錄入:做的時候就記下來嗎?)
- Original (原始:是最源頭的紀錄嗎?)
- Accurate (準確:數據真實嗎?)
「沒有紀錄,就代表沒做過 (Not documented, not done)」,這是 GxP 世界裡的至理名言。
如果你能透視這層邏輯,你就會發現 GxP 不是冷冰冰的條文,而是醫藥產業為了守護那份「生命託付」而編織的嚴密信用網絡。無論你是新進嚮導、戰略指揮官,還是品管建築師,希望這篇文章能讓你重新看見 GxP 的理性之美,並在隨時變動的規則中,穩健地走在通關路徑上。
















