跨越臨床邊界:美國 FDA IND 審查流程與實務全解析
前言:30 天的靜默與博弈
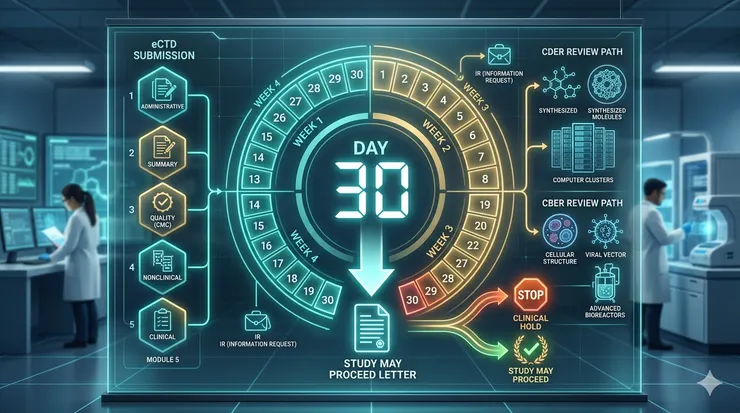
在美國藥品開發的法規框架下,新藥臨床試驗申請(Investigational New Drug Application, IND) 不是一張簡單的「准考證」,而是一道「不反對即許可」的行政門檻。根據美國聯邦法規 21 CFR 312,當廠商遞交 IND 後,會進入一個長達 30 天的審查期。若這三十天內 FDA 未發出暫停指令(Clinical Hold),臨床試驗便可自動合法啟動。
對於 Regulatory Affairs (RA) 職人而言,這三十天並非靜候佳音的空窗期,而是一場高強度的資訊對位 (T.T~~)。我們必須在嚴謹的格點內,確保非臨床數據(Nonclinical)、製造管制(CMC)與臨床計畫(Clinical Protocol)完美銜接,以換取那封關鍵的「Study May Proceed Letter」。
一、 送件要求:建構理性的 eCTD 結構
在美國,IND 的送件早已進入全面數位化的 eCTD (Electronic Common Technical Document) 時代。一份完整的 IND 文件包,通常包含五大模組:
- Module 1:行政資訊與區域需求(如 Form FDA 1571、Cover Letter)。
- Module 2:高品質摘要(最核心的部分,審查員首選閱讀的內容)。
- Module 3:品質文件 (CMC)(試驗藥品的製程、分析方法與安定性等)。
- Module 4:非臨床報告(所有藥理與毒理試驗報告)。
- Module 5:臨床試驗計畫書(臨床試驗計畫書、試驗醫師的 CV 等)。
廠商送件後,FDA 的 Electronic Submissions Gateway (ESG,用來讓藥廠以電子方式安全提交法規文件,並進行基本技術驗證的官方入口平台)會先進行一層「技術性驗證(technical validation validation)」,如果發現技術性錯誤(例如 XML 檔壞掉、檔案命名錯誤、模組放錯位置),廠商會收到 validation failure,此份申請會被拒收。
二、 審查時間與行政時程
- Day 0:成功透過美國 FDA 的 ESG(Electronic Submissions Gateway)完成 eCTD 提交。
- Day 1–7(通常數日內):FDA 完成行政收文並發出 Acknowledgement Letter 及 official receipt date(此日期為 30日審查的起算點)。
- Day 30: 關鍵的決定點。若 30 天內無異議,IND 自動生效。
三、 審查方式:CDER 與 CBER 的異同
美國 FDA 內部根據產品類別,由不同的中心進行審查,其風格與重點略有不同:
1. CDER (藥物評估與研究中心)
- 對象: 化學小分子藥物、多肽、多數單株抗體。
- 審查風格: 流程高度標準化。審查團隊通常包含專案經理 (Regulatory Project Manager, RPM)、藥理毒理學家、化學審查員 (CMC Reviewer) 與臨床醫師。
- 重點: 強調製程的重複性與臨床起始劑量的安全性(Safety of Starting Dose)。
2. CBER (生物製品評估與研究中心)
- 對象: 疫苗、血液製品、細胞治療、基因治療。
- 審查風格: 高度 case-by-case(產品差異大)。
- 重點: 極度關注病毒安全性(viral safety)、效價測定(potency assays)、製程與產品變異性(product variability)。若針對細胞 / 基因治療產品,則特別關注:
- 無菌與污染控制(sterility / adventitious agents)
- 細胞特性與一致性(identity / purity / potency)
- 長期安全性(例如 tumorigenicity)
四、 補件與溝通:Information Request (IR) 的應對
在 30 天審查期間,FDA 審查員若對資料有疑義,會發出 Information Request (IR),並要求申請者在限定的時間內回覆。這不是「不核准」,而是為了避免發出 Clinical Hold 的最後對話機會。
由於這 30 天的審查時間,也包括廠商回覆的時間,在時間上非常地趕。所以,FDA 只要有問題,就會直接丟 IR 過來,不會等到收集完所有 IR 後再一次提供。有時候他們當天上午發一個 IR,然後下午又發一個。因此,遞交 IND 申請後的 30 天,公司團隊會非常緊繃 。
(備註:台灣 TFDA 對 IND 審查的程序也和美國 FDA 完全不同,之後會撰文詳述。)
- 回覆方式: 通常透過電子郵件(由 RPM 轉發)或正式遞交 eCTD 補件。
- 時間壓力: FDA 審查員通常要求在 24-72 小時內 回覆。這要求 RA 團隊具備極強的跨部門協作力,在時限內完成回覆的內容。
(RA 甘苦談:這大概是 RA 壓力值直線飆升的時刻。對台灣公司來說,時差就是最大的敵人。FDA 的 IR 常常在台灣的深夜悄悄寄出。當多數人已進入夢鄉,RA 卻得瞬間切換成戰鬥模式,在第一時間轉發 IR 給內部團隊、同步啟動討論,甚至開始著手撰寫回覆。筆者過去在 IND 送件後,從第二週開始,每天都設好凌晨三點的鬧鐘,只為了在第一時間掌握 FDA 的任何動靜。某種程度上,RA 的生理時鐘,也是在這段期間被「法規化」了。) - 策略對位:回覆 IR 時,關鍵在於「精準命中」審查員的疑慮,而不是把所有資料一股腦地傾倒上去。過多無關的數據,反而可能讓問題越滾越大,甚至引出新的關切點。同時,也要記住一件事,FDA 的每一項要求,並非都需要全盤接受。當某些要求(例如:並無充分依據卻建議增加特定檢測項目)缺乏明確科學基礎時,應該以邏輯清晰、科學合理的論述進行說明與回應,適度地提出不同觀點,來說服 FDA(成為 "push back")。畢竟,好的法規溝通,不只是回覆問題,更是在建立一場有理有據的專業對話。
五、 告知核准與啟動:Study May Proceed
若審查順利,FDA 通常不會以「核准」的概念明確批准 IND,而是採取 no objection(無異議)機制。實務上有兩種情境:
- 默許生效:若在 30 天內未收到臨床暫停 (Clinical Hold) 的通知,IND 即可依法進入臨床階段。但多數廠商仍會主動與 RPM 確認是否可啟動試驗。
- 正式溝通通知(Communication from FDA):由 RPM 以 Email 告知 IND 可進行,這封信稱為 "Study May Proceed" letter。
此外,值得一提的是,取得 "Study May Proceed" letter 雖然代表 FDA 已同意此試驗執行,但通常 FDA 還是會同時提供一份 "Non-hold comments" (其實全世界很多監管機關都會這樣做,很機車)。這份 Non-hold comments 是 FDA 提出的非強制性審查建議或風險提醒 (簡單來說,就是我同意這個試驗可以執行,但是你還要做到/注意點點點.....)。這份文件為 FDA 供申請者參考,並在後續修正或補充說明之用。雖說不影響試驗進行,但有時會有蠻多額外的要求,也會增加團隊的負擔。此外,筆者過去在收到 Non-hold comments 後,也是會提供一份正式的回覆。
六、 不核准執行:Clinical Hold (臨床暫停)
若在 FDA 的 IND 審查過程中,認為受試者可能面臨不合理且顯著風險,或申請資料存在重大缺失,且無法在 IND 審查的 30 天內補足,FDA 就會發出臨床暫停 (Clinical Hold) 信件,信件中,FDA 會明確指出臨床試驗不能進行,並且列出所有缺失。這裡要注意的是,Clinical Hold 信件裡,FDA 不會訂定廠商需要提供回覆的期限,廠商可以自己決定回覆的時間,或是不回覆。
廠商在收到 Clinical Hold 信件後,需針對 FDA 所列缺失逐項回覆,並提供補充資料或修正方案。在 FDA 收到完整回覆後,會啟動新的 30 日審查,如果 認為廠商回覆的內容可接受,就會發出一封 "Remove Clinical Hold Letter" (解除臨床暫停信函),代表 FDA 核准了這個 IND。
但如果 FDA 不接受廠商的回覆,就會以 email 或 IR 等方式,回覆這個 IND 仍維持暫停 (hold) 的狀態。後續廠商仍可以持續提交補充資料,FDA 也會進行審查。這整個循環,在法規上並沒有明確「次數上限」,但若問題反覆無法解決,並且時間拖得太久,FDA 有可能要求重大的設計變更,最嚴重可能會要求重新遞交 IND 申請 (但少見)。
(備註:台灣 TFDA 對 IND 審查的程序也和美國 FDA 完全不同,之後會撰文詳述。)
結語:理性的格點,感性的共識
IND 審查不是一場冰冷的法律攻防,而是廠商與監管機構之間,針對「科學風險」與「患者獲益」的共識達成過程。身為 RA 職人,我們在 eCTD 的每一個模組中佈下的不只是數據,更是「可信度」。
當我們能精準預測審查員的考量、靈活應對 IR 的快節奏,並在三十天內達成完美的對位,這不只是法規上的通關,更是為全球患者爭取到了一個新希望的起跑機會。
-------------------------------------------------------------------------------------------------------
本文內容僅供資訊分享與學術討論之用,不構成任何法律、法規諮詢、專業建議或針對特定專案的指導。文章中所提及之內容(如美國 FDA 審查流程、時間及實務操作等)均基於筆者個人實務經驗與撰文時現行之公開法規資訊;由於法規環境可能隨時異動,相關實務細節仍應以監管機構(如 U.S. FDA)發布之最新官方公告及指引(Guidance)為準。
-------------------------------------------------------------------------------------------------------




















