
法說會簡報:https://mopsov.twse.com.tw/nas/STR/694520260416M001.pdf
蛋白質藥研發企業在次世代雙特異性抗體領域取得關鍵進展,其自主開發的研發平台已成功轉化為具備國際競爭力的臨床數據。透過精準鎖定致病途徑並降低傳統療法的副作用,該公司不僅在眼科高階市場建立起技術壁壘,更透過靈活的授權模式確保研發資金的持續性。隨著核心管線進入商業化前夕,市場評價正從單純的研發成本投入,轉向對平台授權價值的實質認列。
一、 近期營收動態分析 :
- [2026 年 3 月] 單月營收:0 元;月增率 (MoM):0 %;年增率 (YoY):0 %。
- [2026 年 2 月] 單月營收:0 元;月增率 (MoM):0 %;年增率 (YoY):0 %。
- [2026 年 1 月] 單月營收:0 元;月增率 (MoM):0 %;年增率 (YoY):0 %。
- [2026 年 1 至 3 月] 累計營收:0 元,較去年同期成長 0 %。
【財報指引】: 公司目前處於新藥研發階段,營收認列採里程碑金制度 (Milestone payments)。2025 年全年營收為 0 元,目前營運資金充裕,主要支出集中於臨床試驗與專利佈局。
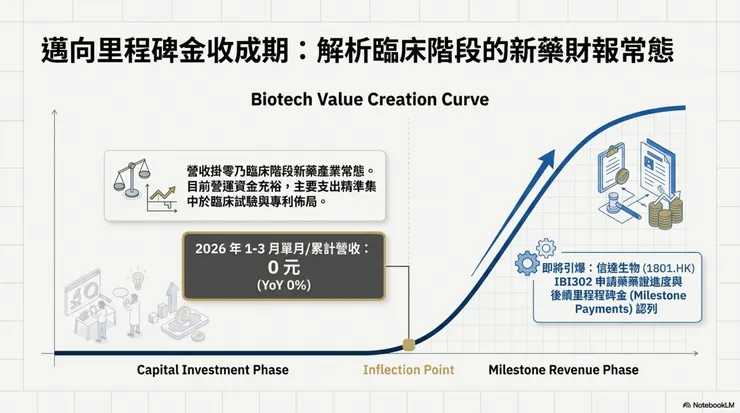
數據解讀: 筆者認為,對於處於臨床階段的新藥研發公司,單月營收為 0 元乃是產業常態,並非營運不佳。投資重點應聚焦於 IBI302 三期成功後,合作夥伴信達生物 (1801.HK) 申請藥證之進度,以及後續隨之而來的里程碑金認列。營收爆發點將取決於授權合約的簽署與臨床階段的跨越。
二、 核心業務與產品結構分析
營收佔比:目前尚無產品上市銷售,價值全數由研發管線支撐。
核心技術與護城河:
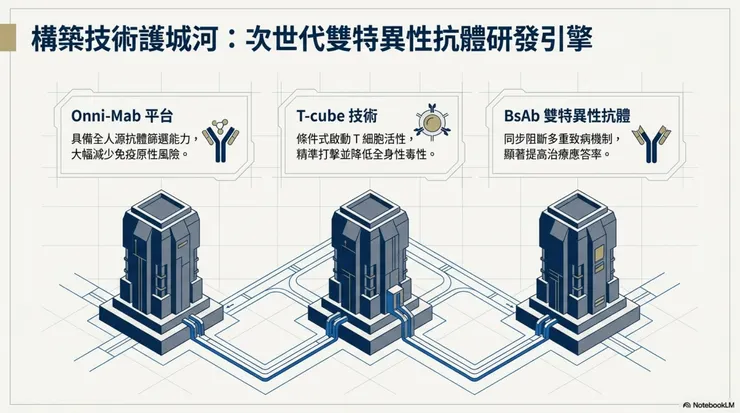
- Omni-Mab 平台:具備全人源抗體篩選能力,減少免疫原性風險。
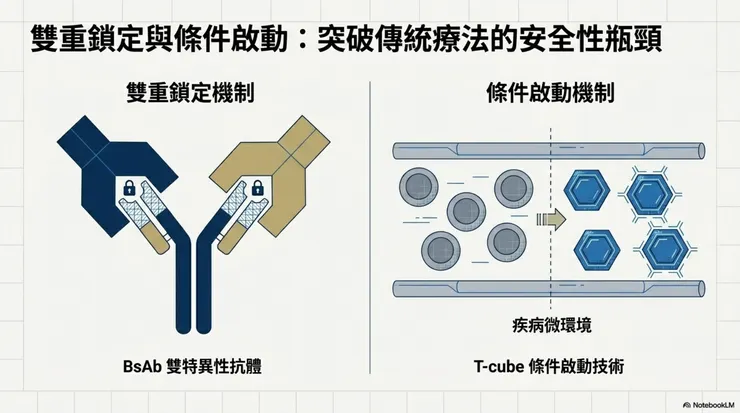
- T-cube 技術:條件式啟動 T 細胞活性,降低全身性毒性。
- BsAb 雙特異性抗體:同步阻斷多重致病機制,提高治療應答率。
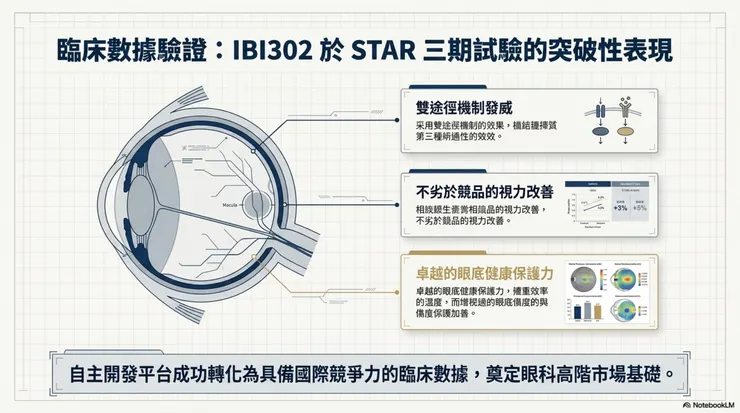
三、 技術分析:IBI302 雙途徑機制與臨床優勢
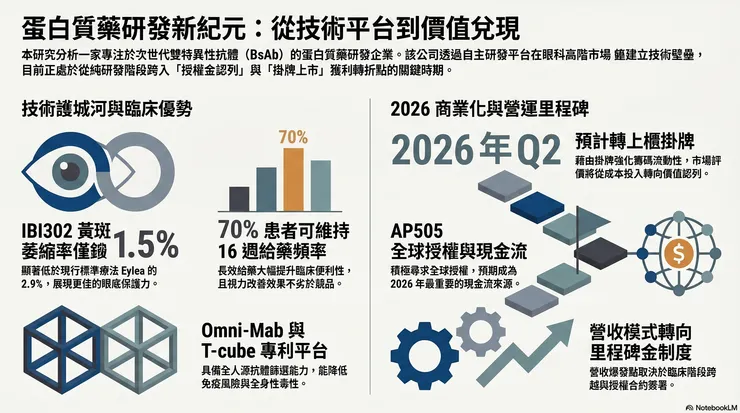
分析目標: IBI302 在 STAR 三期試驗展現顯著優勢,其黃斑部萎縮 (MA) 發生率僅 1.5 %,遠低於現行標準療法 Eylea 的 2.9 %。在維持視力改善不劣於競品的同時,展現了更好的眼底健康保護力。此外,超過 7 成患者可維持 16 週一次的長間隔給藥,大幅提升臨床便利性。

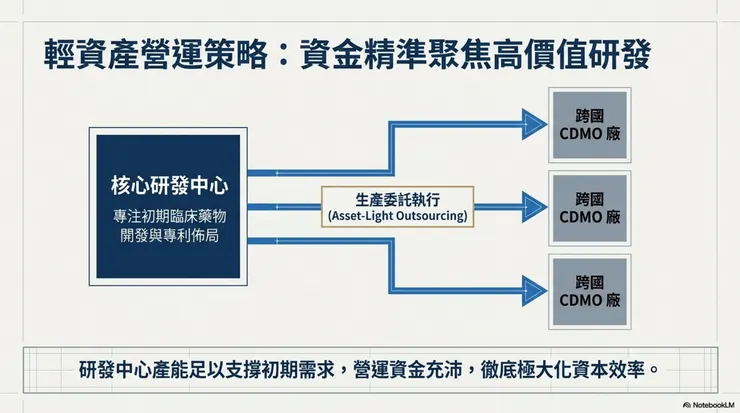
四、 未來展望與產能佈局
產能規劃: 公司採輕資產模式,生產委託跨國 CDMO 廠執行。目前研發中心產能足以支撐初期臨床所需藥物開發。
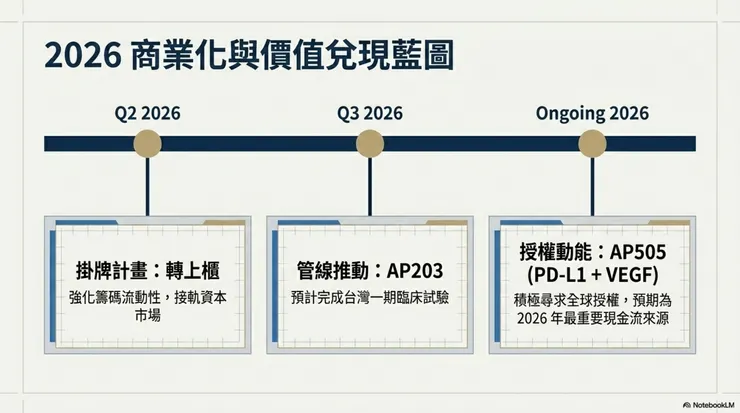
營運指引:
- 掛牌計畫:預計 2026 年第 2 季完成轉上櫃,強化籌碼流動性。
- 授權動能:AP505 (PD-L1 加 VEGF) 積極尋求全球授權,預期為 2026 年最重要現金流來源。
- 管線推動:AP203 預計 2026 年第 3 季完成台灣一期臨床試驗。
五、 投資觀點整理
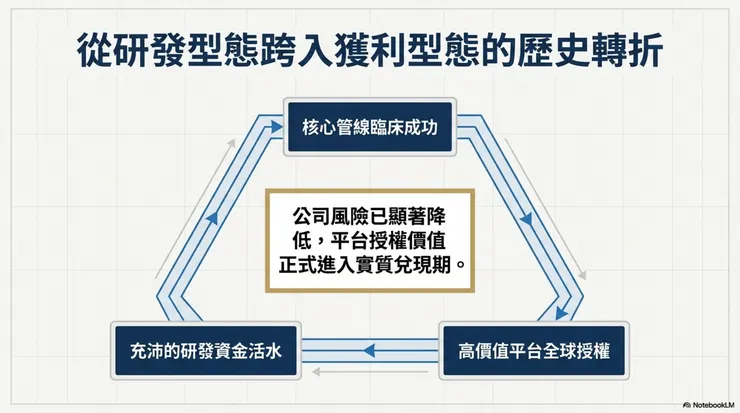
結論:核心管線的臨床成功已將公司風險顯著降低,平台授權價值即將進入兌現期。 筆者觀察,雖然目前月營收呈現掛零狀態,但其技術護城河已透過三期臨床數據獲得全球藥廠關注。隨著 AP505 進入二期臨床並尋求授權,加上 2026 年轉上櫃的里程碑,公司正處於從研發型態跨入獲利型態的轉折點。
六、 法說會 Q&A 整理
Q1:2026 年第 1 季營收為 0 元,是否影響轉上櫃進度?
A1:生技新藥掛牌重點在於技術價值與臨床進度,目前上櫃申請程序照計畫進行,不受短期營收數字影響。
Q2:IBI302 在中國市場的競爭壓力為何?
A2:IBI302 是全球首創雙途徑藥物,具備減少黃斑部萎縮的獨特優勢,在同質化嚴重的抗 VEGF 市場中具備高度差異化。
Q3:AP505 目前的授權談判進度?
A3:目前與多家國際大藥廠洽談中,公司目標是在 2026 年內達成具備里程碑意義的國際授權協議。
Q4:公司目前現金流量可支撐多久?
A4:現有資金足以應付 2026 全年研發需求,配合轉上櫃籌資與潛在授權金,資金鏈極為穩健。
Q5:T-cube 平台是否會授權給其他公司使用?
A5:公司對平台授權持開放態度,除了管線授權,未來不排除進行技術平台共同開發。
Q6:IBI302 申請藥證的時間點?
A6:信達生物預計近期將向中國 NMPA 提交申請,具體進度依監管機構審核為準。
Q7:未來是否有自行建廠的規劃?
A7:目前仍維持輕資產委外生產模式,將資源集中於最具價值的藥物設計與臨床試驗。
免責聲明:容僅供參考,不構成任何投資建議。生技產業具備高度開發風險,投資人應獨立評估。





















