【市場脈動|為何一份數據讓禮來股價大跌】
2025/8/7,禮來(Eli Lilly)第二季營收 156 億美元(年增 38%),淨利 56.6 億美元(年增 60%)。王牌替爾泊肽 Tirzepatide(Zepbound/Mounjaro)上半年銷售 147.3 億美元,第二季已超越司美格魯肽 Semaglutide(Wegovy/Ozempic),今年很可能成為新藥王。然而,禮來股價單日下跌 14%,主因是口服 GLP-1 受體小分子激動劑 Orforglipron 三期減重數據不如市場期待,凸顯「口服減重藥」的商業敏感度與戰略價值。【為什麼「口服」這麼關鍵】
目前多數強效減重藥物屬於胜肽類、以皮下注射給藥。若能以口服小分子達到接近或超過注射劑的體重下降與代謝效益,將在依從性、可近性、製造與供應鏈效率上形成明顯優勢,也更容易觸及更大的一般醫療市場。
【Orforglipron 三期要點(orforglipron)】
在 72 週主要試驗中,高劑量 36 mg 以「安慰劑校正」計算的減重幅度為 11.5%;中劑量 12 mg 為 8.4%。所謂「安慰劑校正(placebo-adjusted)」是將藥物組的變化扣除安慰劑組的變化,更貼近藥物的純粹效應。需留意目前沒有與口服司美格魯肽的頭對頭(head-to-head)隨機對照,跨試驗比較僅具參考性。
【與口服司美格魯肽對照(Oral Semaglutide)】
已公開資料顯示,口服司美格魯肽 25 mg 在 64 週的減重為 13.9%;50 mg 為 15.0%。相較之下,Orforglipron 36 mg 在 72 週為 11.5%。雖然試驗設計、族群與週期不同不可直接等同,但就「口服對口服」的觀感而言,差距並未到難以挽回的程度。安全性方面,兩者主要不良反應集中在胃腸道(噁心、嘔吐、腹瀉),與 GLP-1 類機制一致。實務判讀時,還需考量劑量遞增速度(titration)、基線體重與生活型態介入等差異。
【口服 GLP-1R 小分子賽道仍擁擠】
臨床階段中仍有逾 30 個 GLP-1R 小分子候選在推進。雖然 Orforglipron 未達預期,但「後發領先」在藥物史上並不少見(類比他汀市場中後來居上的 Atorvastatin/Lipitor)。接下來的競爭重點,將是誰能在有效性、耐受性與劑量遞增策略上找到最佳平衡。
【胰澱素線崛起:諾和諾德 Amycretin 與 CagriSema】
Amycretin(amycretin)同時鎖定 GLP-1 與胰澱素(Amylin)。胰澱素由胰臟 β 細胞分泌,可抑制食慾、延緩胃排空並調節餐後血糖,與 GLP-1 作用互補。 皮下劑型:Ib/IIa 期中,20 mg 於 20 週可見最高約 22% 減重;後續在 ADA 場合更新至 36 週約 23.9%。 口服劑型:I 期 12 週平均減重約 13.1%,安全性與耐受性整體良好。 開發節奏:諾和諾德已規劃皮下與口服並進到肥胖與糖尿病的後期開發,但未公布 III 期時間表。 相關的雙機制注射 CagriSema(cagrilintide + semaglutide)在 2024/12 讀出後市場反應不如預期,顯示高期望下的風險敞口仍在。
【同場競速:Viking VK2735(GLP-1/GIP 雙靶)】
VK2735(VK2735)機制與禮來的 Tirzepatide 類似,布局皮下與口服兩條線。口服 I 期短期數據顯示:40 mg 連續 28 天相對安慰劑平均減重約 3.3%;最高 100 mg 28 天平均減重約 8.2%。II 期 VENTURE-Oral(每日一次,N=280)已完成入組,官方預期 2025 下半年提供數據。若後續證實維持高效且耐受性可控,將直接抬高口服賽道的天花板。
【羅氏/基因泰克 Carmot 資產:CT-996(偏向性 GLP-1)】
CT-996(CT-996)主打 GLP-1 受體「偏向性(biased)訊號傳遞」,嘗試在保留療效的同時改善耐受性。Ib 期 4 週顯示減重約 7.3%(安慰劑約 1.2%)。但 2024 年歐洲糖尿病研究協會會上,快速劑量遞增族群出現較高比例的胃腸副作用(噁心、嘔吐、腹脹、便祕等)。後續計畫補充 I 期並推進有無糖尿病的肥胖族群 II 期。這提示「titration 策略」極可能是口服 GLP-1 類藥物耐受性的關鍵槓桿。
【機制差異化:Rhythm Bivamelagon(MC4R 致效劑)】
Bivamelagon(bivamelagon)直接作用於黑皮質素-4 受體(MC4R),該路徑位於中樞神經,主司食慾與能量平衡,過去多見於罕病領域。II 期在獲得性下丘腦肥胖症(HOb)顯示:400 mg 14 週 BMI 下降約 7.7%,600 mg 約 9.3%,安慰劑約 2.2%。曾出現直腸出血(導致停藥)與局部色素沉著過度等訊號,需在後期持續監測。公司計畫與美/歐監管機構討論 III 期路徑。
【臨床與商業解讀:五個關鍵抓手】
- 口服效能門檻正成形:若在 64–72 週能達約 12–15% 減重且耐受性可控,即具商業競爭力;若能突破 15%,才可能正面挑戰注射皇牌。
- 劑量遞增策略決定耐受性:快速 titration 可能提高胃腸道不良反應與停藥風險;最佳化遞增與輔助處置(如抗噁心方案)是差異化重點。
- 雙/多靶點趨勢確立:GLP-1 + 胰澱素(Amycretin/CagriSema)、GLP-1 + GIP(VK2735)等,可同時影響食慾、能量代謝與胃排空,多軸驅動效能上限。
- 小分子與胜肽並非零和:短中期更可能形成分層分流與聯合治療;小分子強在口服便利與擴張性,胜肽強在高效與既有證據體系。
- 誰是口服王者仍待頭對頭:未來需 H2H 試驗或真實世界數據(RWD)來定勝負,尤其在長期維持、代謝合併症改善與停藥後反彈等面向。
GLP-1RA:模擬腸促胰素 GLP-1,抑制食慾、延緩胃排空、促進胰島素分泌。 GIP:另一種腸促胰素,與 GLP-1 並用常見於雙靶策略。 胰澱素(Amylin):胰臟 β 細胞分泌,抑制食慾、延緩胃排空、平抑餐後血糖。 MC4R:中枢路徑,調控飢餓與能量消耗。 安慰劑校正:扣除安慰劑組變化後的藥物純效應估計。 偏向性致效(biased agonism):同一受體偏好啟動特定訊號路徑,以期兼顧效能與耐受。
【研發偵查與專利洞察(不涉特定品牌)】
以公開專利資料結合計算工具,可快速圈定候選藥物可能對應的核心專利,萃取成藥性數據(效力、選擇性、ADME 等),統計高頻母核/片段以推估結構—活性關係(SAR),並輸出 SDF 交由化學繪圖軟體重建實施例結構。針對 Amycretin、VK2735、CT-996 等,可用此路徑比對公開專利族群、解析設計趨勢,並回扣至臨床耐受性(特別是胃腸道事件)以調整分子與給藥策略。
【結語】
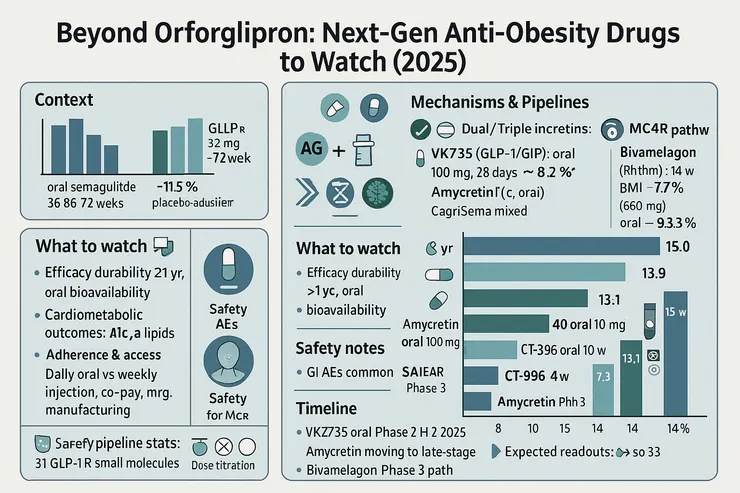
Orforglipron 的三期數據未臻預期,卻把「口服小分子 GLP-1」的門檻與痛點更清楚地呈現出來。接下來值得持續關注的主角包括:Amycretin(GLP-1/胰澱素雙機制)、VK2735(GLP-1/GIP 雙靶)、CT-996(偏向性 GLP-1 口服)、以及走差異化中樞機制的 Bivamelagon(MC4R)。真正的口服王者,仍有待後續頭對頭試驗與長期真實世界證據定錨。
---
參考資料:
- 公司官網&公開資料
- https://www.biospace.com/drug-development/5-oral-obesity-drugs-challenging-lillys-orforglipron.

























