※如欲轉載本文,請移步至北美智權報「聯絡我們」頁面填寫表單與我們聯繫
林杜 / 永信藥品法規處專員新藥開發公司在進入臨床試驗前,由於自己沒有劑型開發與製造的能力,通常會委外合作。由於臨床三期的費用通常是臨床二期的 3–5 倍,甚至更高,新藥開發公司通常會在臨床二期看到療效後,尋求授權。一項藥品要能夠成功上市,過程中必需有許多合作,此時智慧財產權的管理就顯得相當重要,Merck Serono v. Hopewell Pharma 案發生的問題可做為借鏡。
案件背景
2025年10月30日,聯邦巡迴法院維持了專利審判暨上訴委員會(Patent Trial and Appeal Board, PTAB)的裁定,宣告 Merck 旗下多發性硬化症藥物 Mavenclad(化合物 cladribine 的口服劑型)的專利權利範圍無效。這份具先例價值的判決維持了多方複審(IPR)的結果,判定 Merck 主張的 cladribine 治療法專利無效,支持了挑戰者 Hopewell藥廠。
本案的核心爭議點在於:PTAB 據以認定「顯而易見性」(Obviousness)的主要引證文件,是否構成 Merck 專利的先前技術(Prior Art)。由於該引證文件的公開日期比 Merck 提交申請的日期早不到一年,Merck 主張該公開內容實際上是出自其自身部分發明人之手,因此不應視為先前技術。
Merck 的前身 — 新藥開發公司 Serono 公司[1]於2002年時與製造商兼劑型開發商 Ivax 公司[2]合作開發 cladribine 的口服劑型。Serono 公司向 Ivax 公司發送了一份「簡報文件」,Ivax 公司的員工 Bodor 博士與 Dandiker 博士卻將「簡報文件」中的給藥方案寫入其申請的專利中(後簡稱 Bodor專利),而Bodor 專利後來成為了 Hopewell 用來攻擊 Merck 專利的主要引證,最終導致 Serono 公司的 ’947 專利被判無效。[3]
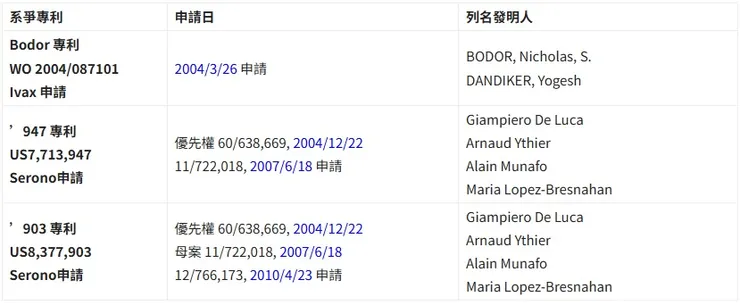
表1. Ivax 公司及Serono 公司涉案相關專利申請時序;整理製表:北美智權報/林杜
此文未完,完整內容請參見原文連結。
【更多專文報導請見《北美智權報》401期;歡迎加入NAIPNews網站會員成為我們的訂戶,以掌握最關鍵的專利商標智財消息!】















