【真正吞噬專案的,從來不只是不夠努力】
創新藥研發最殘酷的地方,不在於它難,而在於你往往在一開始就知道,它極可能失敗,卻還是必須投入多年時間、巨額資本,以及一整個團隊的職業生涯去把它往前推。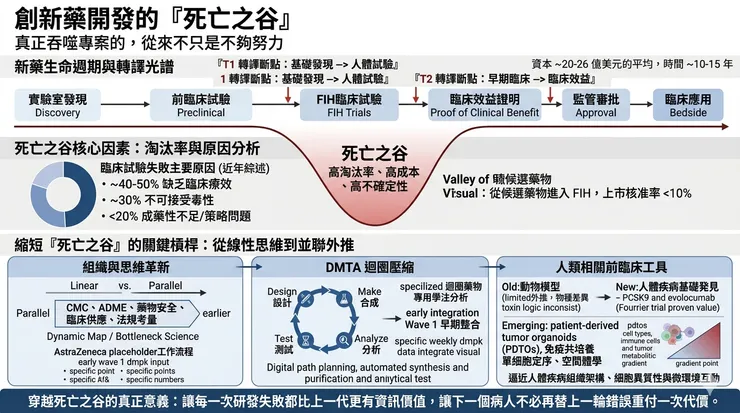
所謂「死亡之谷(Valley of Death)」之所以在生技醫藥圈反覆被提起,正是因為它不是一句危言聳聽的行話,而是整個產業最真實的結構性命題:從一個在實驗室裡看起來很有希望的發現,到真正成為能改變病人命運的藥物,中間隔著的不是單一道門檻,而是一整片高失敗率、高成本、高不確定性的無人區。
「死亡之谷」這個比喻本來就不是生醫圈獨有的詞。它在 1990 年代美國的科技政策與創新融資討論中逐漸成形,1998 年美國國會《Unlocking Our Future: Toward a New National Science Policy》已明確用它來描述基礎研究與產業化之間那段最容易失血、也最容易失去支持的斷裂帶;到了 2008 年,Nature 以〈Crossing the valley of death〉為題討論生醫轉譯困境後,這個概念才真正進入今日大家熟悉的「從 bench 到 bedside」語境。
後來,轉譯醫學又把它進一步拆得更細:不只是一個谷,而是沿著 T1、T2、T3、T4 轉譯光譜分布的多重斷點;其中最核心、最致命的,依然是 T1 與 T2,也就是從基礎發現走到人體試驗,以及從早期臨床走到真正證明臨床效益的兩大關口。
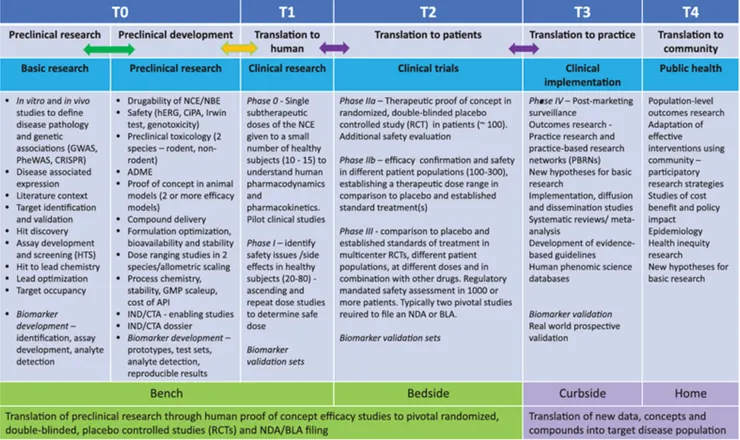
✦【這條谷,為什麼總是這麼難過?】
如果把這條谷量化來看,它的殘酷程度其實比大多數人想像得更高。
多篇近年綜述都指出,從候選藥物進入人體試驗開始算,最終能走到核准上市的比例通常仍不到一成;若把前端臨床前淘汰也一併算進去,整體淘汰率只會更高。另一方面,把一個新藥從發現推到市場,常見估計仍落在 10 至 15 年、約 20 億至 26 億美元等級;而且這還只是平均數,並不代表每一個失敗專案都能在早期低成本地被及時止損。
更值得注意的是,2025 年 Nature Communications 的動態成功率分析也提醒大家:所謂「成功率」不是固定常數,不同疾病、不同模態、不同開發策略差異很大,但整體臨床成功率長期仍只在個位數到兩成之間波動,而 Phase II 持續是最難穿越的一段。
為什麼這條谷總是這麼難過?原因其實不神祕,但非常殘酷。
最常見的失敗理由,第一仍是缺乏臨床療效,大約占 40% 到 50%;第二是不可接受的毒性,大約 30%;再往後才是成藥性不足,例如溶解度、暴露、代謝穩定性等藥物樣特性問題,以及商業與策略因素。
換句話說,多數專案不是死於「沒有做到」,而是死於「在人體裡沒有像原本以為的那樣成立」。這也是為什麼死亡之谷從來不只是執行問題,而是預測問題。

✦【真正讓預測失靈的,是生物學本身】
而預測失靈的核心,往往就來自生物學本身。
過去藥廠與學界太習慣把動物模型當成人體的縮影,但實際上,物種差異、疾病模型失真、腫瘤微環境不完整,以及毒性機制在人與動物間的不一致,早就反覆削弱了這種假設。回頭看文獻,對動物與人體毒性一致性的評估其實並不樂觀;有些回顧甚至指出,許多跨物種預測能力只比隨機好一些。
這不是說動物實驗沒有價值,而是說它只能提供「有限且條件性的訊號」,遠遠不足以保證人體結果。也正因如此,從動物有效到人體有效,仍是死亡之谷裡最深的一段。
更麻煩的是,就算你拿到的是一個機制漂亮、遺傳學支持強的標靶,也不代表臨床價值會自動落地。
像 evolocumab(Repatha)這類針對 PCSK9 的藥物,背後的人類遺傳學與機制邏輯都相當強,但它真正站穩臨床地位,靠的仍不是機轉推理本身,而是 FOURIER 這類大型臨床結果試驗去證明它確實能降低主要心血管複合終點。
這個例子真正提醒產業的,不是「好標靶也可能失敗」,而是「從好生物學走到可支付、可複製、可被臨床社群接受的真正價值,中間永遠需要更高層級的人體證據」。
✦【死亡之谷,不只是科學問題】
所以,死亡之谷絕對不只是科學問題,它同時也是資本問題、組織問題與法規問題。
在資本面,早期風險最高時,商業資本往往最猶豫;到了後期風險相對下降,資金需求卻又陡然放大,形成典型的時間錯配。這也是為什麼美國長期用 SBIR、NCATS 這類轉譯資源去填補早期無人承接的地帶:不是因為市場不重要,而是因為很多案子在形成可投資性之前,就已經先死在缺乏橋接資金與轉譯基礎設施的階段。
在組織面,死亡之谷則常常是被「線性思維」放大的。藥物開發本來就不是化學、生物、藥理、毒理、製劑、CMC、臨床與法規各跑各的接力賽,但很多組織實際運作起來,仍像在打分段外包。
結果就是:
- 前端只顧 potency,後端才發現暴露不對。
- 先把分子做出來,後面才發現放大量產根本不可行。
- 等到要進 IND 或 FIH 才回頭補 developability。
近年轉譯科學之所以反覆強調「dynamic map」與「bottleneck science」,正是因為要把這種舊式串聯流程改成更早期的並聯思維,讓 CMC、ADME、藥物安全、臨床供應與法規考量更早進入候選物選擇。
✦【真正縮短死亡之谷的,不是更努力,而是更早知道自己錯在哪裡】
同樣的轉變,也發生在藥物研發最核心的 DMTA(Design–Make–Test–Analyze)迴圈上。
今天沒有人再把 DMTA 當成一條單純的化學工作流;它更像是一套用來壓縮認知錯誤與試錯成本的決策機器。像 AstraZeneca 公開的工作流程就顯示,他們把早期 DMPK Wave 1 的整合測試前移,幾乎以每週節奏把脂溶性、溶解度、蛋白結合與代謝穩定性等資訊回灌到分子設計;而近年的綜述也都把自動化合成、數位化路徑規劃、純化與即時分析,視為縮短 DMTA 週期的關鍵槓桿。
意思很簡單:死亡之谷不可能靠「更努力」被填平,它只能靠更早知道自己錯在哪裡來縮短。
✦【更人類相關的工具,正在讓這條谷慢慢變窄】
真正有機會改寫這條谷形狀的,還有一類更人類相關的前臨床工具。
過去幾年,patient-derived tumor organoids(PDTOs)、免疫共培養、單細胞定序與空間體學快速成熟,最大的意義不是「技術更炫」,而是它們讓我們第一次比較像樣地逼近了人體疾病的組織架構、細胞異質性與微環境互動。
近年的綜述已經相當一致地認為,PDTOs 在標靶驗證、藥效預測與前臨床分層上愈來愈有價值;而空間體學則進一步把細胞位置、細胞互作、代謝梯度與腫瘤生態系統拉回分析框架。若再和免疫共培養、器官晶片與多模態資料整合放在一起,轉譯研究的「人類相關性」確實正在被往前推。
這並不代表死亡之谷會消失,但至少代表未來有更多工具可以讓它變窄。
✦【法規不是最後一道關,而是一路同行的條件設定者】
法規面也一樣。
很多人把監管看成最後一道關,其實它更像一路同行的條件設定者。尤其在細胞治療、基因治療與腫瘤加速核准等領域,近年最明顯的特徵不是「放鬆」或「收緊」這麼簡單,而是證據要求與彈性機制同步演化:
- 🌿 一方面,FDA 近年持續要求加速核准後的 confirmatory trials 必須更及時、更有能力驗證真正臨床效益。
- 🌿 另一方面,對細胞與基因治療這類製造與臨床設計都高度特殊的產品,FDA 也持續透過新指引與彈性 CMC 路徑去降低不必要的制度摩擦。
這說明了一件很重要的事:死亡之谷的一部分,其實是制度與技術節奏不同步造成的。
✦【如何跨越死亡之谷?答案從來不是單一解法】
所以,今天再談「如何跨越死亡之谷」,答案早就不可能是單一解法。它不是再去找一個更會講故事的 CEO,也不是把 AI 貼到每一張簡報上,就能把問題自動解決。
真正有效的路徑,通常同時包含幾件事:
- 🌱 更早期、也更嚴格的人體相關標靶驗證。
- 🌱 把化學、DMPK、毒理、製程與臨床供應前移整合。
- 🌱 用更高密度的 DMTA 去縮短錯誤暴露時間。
- 🌱 用 PDTO、單細胞與空間體學提升前臨床外推能力。
- 🌱 用 bridge funding、轉譯平台、共研授權與法規科學把最危險的空窗帶補起來。
死亡之谷無法靠單點突破被征服,它只能靠整條價值鏈一起變聰明。

✦【寫在最後】
最後必須說,死亡之谷從來沒有真正消失過。它只是隨著模態改變而不斷換臉。
小分子藥曾經卡在 ADME 與 selectivity;後來 ADC 要處理 linker、payload 與耐受性;細胞治療與基因編輯又把製造、可比性、長期追蹤與病人分層問題重新推到檯面上。
也就是說,創新藥研發不會有一個徹底「沒有死亡之谷」的年代。真正的進步,只會是我們愈來愈早看見風險、愈來愈快修正模型、愈來愈少把病人的時間浪費在根本不該進人體的案子上。
從這個角度看,穿越死亡之谷的真正意義,從來不只是讓藥上市,而是讓每一次研發失敗,都比上一代更有資訊價值;讓下一個病人,不必再替上一輪錯誤重付一次代價。
--------------
參考資料:
[0]: 各公司官網&公開資料
[1]: https://www.ncbi.nlm.nih.gov/sites/books/n/nap12543/ch1/ "Introduction - Venture Funding and the NIH SBIR Program - NCBI Bookshelf"
[2]: https://www.nationalacademies.org/read/9737/chapter/4 "Read \"Materials in a New Era: Proceedings of the 1999 Solid State Sciences Committee Forum\" at NAP.edu"
[3]: https://pmc.ncbi.nlm.nih.gov/articles/PMC11909971/ "Integrating artificial intelligence in drug discovery and early drug development: a transformative approach - PMC"
[4]: https://pmc.ncbi.nlm.nih.gov/articles/PMC9136610/ "Structure‒tissue exposure/selectivity relationship (STR) correlates with clinical efficacy/safety - PMC"


