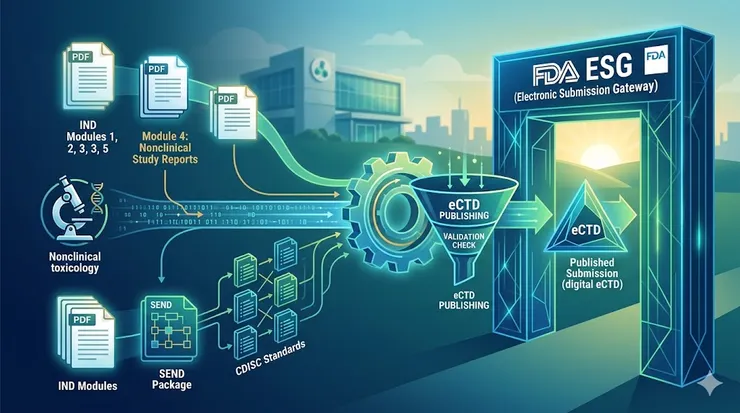
在美國 FDA 的 IND 審查世界裡,一份高品質的送審文件(Submission Package)就像是一座結構嚴謹的建築。我們遞交的每一份 PDF,都必須在 eCTD (Electronic Common Technical Document,通用技術文件) 的框架下,精確地找到自己的格點。
對於 RA 職人而言,準備 IND 文件不只是收集實驗報告,而是把所有的文件,都放在合適的 eCTD 的五個模組(Modules)之下,並在文件之間建立強大的連結。當 FDA 的審查員打開您的送審包時,我們希望他看到的不是紛雜的數據,而是一個「理性的對位」。
一、 誰能發起 IND 申請?(Sponsor 資格與海外廠商規範)
在正式進入文件結構前,我們必須先釐清「試驗委託者(Sponsor)」的法律身分。
- 試驗委託者 (Sponsor) 的定義
根據美國的 21 CFR 312.3,Sponsor 是指對臨床試驗負有法律責任的個人、製藥公司、政府機構或組織。Sponsor 不必是藥物的擁有者,但必須是負責啟動並承擔試驗合規性的人。
- 海外公司 (Foreign Sponsor) 的挑戰
如果您是一家位於美國境外的公司(例如台灣的生技公司),您依然可以作為 IND 的 Sponsor,但 FDA 有一項強制的法律要求:您必須委任一名美國代理人 (U.S. Agent)。
- 美國代理人 (U.S. Agent) 的角色
根據法規,海外申請人必須在美國境內擁有一名代表,其職責包括:
- 溝通窗口: 作為 FDA 與海外 Sponsor 之間的主要聯繫人,負責接收 FDA 的正式信函、IR (Information Request) 或電話通知。
- 法律文件簽署: U.S. Agent 通常需在 Form FDA 1571 上簽署,確認其作為代理人的身分。
- 即時應對能力: 由於審查期間(尤其是那關鍵的 30 天)時常有緊急補件需求,U.S. Agent 最好具備專業的法規知識,協助海外 Sponsor 在時差壓力下完成補件的要求。
職人筆記: U.S. Agent 可以是您在美國的分公司、專業的法規顧問公司 (CRO),或是指定的個人。選擇具備科學背景或醫藥法規專家作為海外公司在美國的代理人,能顯著提升與審查員溝通的效率。
二、eCTD 的骨架:五大模組的導航地圖
FDA 要求所有 IND 都必須以 eCTD (通用技術文件) 的格式遞交。這 eCTD 是一套國際通用的文件格式標準,目的是讓各國的審查員能夠很快地找到特定文件的所在位置,以加速審查的效率。
eCTD 將文件分為五大模組 (Module):
1. Module 1: 行政資訊與區域需求 (Administrative Information)
Module 1 是 IND 送審包的「門面」,包含了所有與行政程序相關的文件。由於 Module 1 大多是行政類文件,因此,它是 eCTD 中唯一讓各國監管機關自行決定文件內容的模組,而每個國家規範的 Module 1 內容都不太一樣。在美國的初始 IND (initial IND) 送件中,Module 1 大致會包括以下文件:

2. Module 2: 通用技術文件摘要 (Summaries)
這是審查員最先閱讀、也最重要的部分。它不是簡單的複製貼上,而是對後續 Module 3、4、5 內容的「精煉」。Mlodule 2 的章節很多,但針對初始 IND 送件,通常只需要遞交下列章節的內容:
- Module 2.2 - CTD Introduction (引言):關於藥物基本資訊、作用機轉及開發背景的精簡導讀,旨在讓審查員在進入技術細節前,快速掌握該新藥的身分與研發定位。
- Module 2.3 - Quality Overall Summary (品質概要):藥品的製造與管制資料的精華,說明藥品的製程及各項特性,以及生產設施。
- Module 2.4 - Nonclinical Overview (非臨床總論):所有非臨床試驗,包括藥理與毒理試驗的綜合評估,核心在於證明「安全性邊際(Safety Margin)」。
職人筆記:在 FDA 的初始 IND 送件中,並不需要提交 Module 2.5 (Clinical Overview 臨床總論),但在中國的初始 IND 送件中,Module 2.5 是必要送審文件。
3. Module 3:品質文件 (Quality / CMC)
Module 3 是技術文件的核心,詳細記載了藥物的 CMC(化學、製造與管制)資訊。其內容涵蓋原料藥與藥品的製程開發、特性鑑定、規格檢驗與安定性數據,旨在證明藥物能在受控的品質標準下穩定生產,並確保每一批次用於臨床試驗的產品都具備一致的安全性與藥效。Module 3 的主要內容包括下列章節:
- Module 3.2.S (Drug Substance,原料藥): 原料藥的來源、製程、特性鑑定與安定性。
- Module 3.2.P (Drug Product,成品): 最終藥品的配方、包裝、滅菌方式與效價試驗。
- Module 3.2.A (Appendices,附錄): 用來存放那些不屬於 3.2.S 及 3.2.P 等常規章節,但對品質評估至關重要的特殊技術資料,例如設施與設備、外源因子安全性評估、新型賦形劑 (Novel Excipients) 等。
- Module 3.2.R (Regional Information,區域性資料):存放符合各國監管機構(如美國 FDA、歐盟 EMA)特定區域法規要求的技術文件。對於 美國 FDA IND 申請案,其核心內容主要包含批量紀錄摘要 (Batch Records)、方法驗證方案 (Method Validation Package)、比較表 (Comparability Protocols)。
4. Module 4: 非臨床報告 (Nonclinical Study Reports)
這是支持 FIH (First-in-Human) 最重要的科學基石。針對初始 IND 申請案,Module 4 的內容通常包括以下章節。申請者可以將所完成的非臨床報告,依其性質放置在合適的章節內。
- Module 4.2.1 (Pharmacology,藥理學)。
- Module 4.2.2 (Pharmacokinetics,藥動學)。
- Module 4.2.3 (Toxicology,毒理學)。
職人筆記 1:請留意毒理試驗 (Toxicology) 和安全性藥理試驗 (Safety Pharmacology) 的執行,需要在有 GLP 認證的實驗室執行。各國監管機關在審查 IND 時,通常會要求申請者提供執行這些試驗單位的 GLP 認證。
職人筆記 2:請留意毒理學(toxicology)且為 GLP 試驗的研究結果,通常需要以 SEND(Standard for Exchange of Nonclinical Data)的格式遞交。SEND 是由 Clinical Data Interchange Standards Consortium 制定的一種標準化資料格式,用於將非臨床(尤其毒理)試驗數據以一致結構提交給 U.S. Food and Drug Administration 進行審查。
5. Module 5: 臨床報告與計畫 (Clinical Study Reports)
雖然 IND 遞交時尚未有臨床數據,但此處需包含:
- Clinical Protocol: 試驗計畫書,這是 30 天審查期的攻防重點。
- 試驗醫師 (PI) 的簡歷。
- FDA Form 1572:由 FDA 制定的文件,用於臨床試驗中由試驗主持人簽署,承諾遵守法規並說明試驗場地、研究團隊與資格。
請留意在 FDA 的法規中,Form 1572 並非 IND 申請時的必要文件,但有時 FDA 的審查員會要申請者提供,因為 FDA 希望申請者會 "真的" 會在美國執行這個臨床試驗,而不是將此 IND 別有它用的 "幌子" (例如用於加速其他國家的審查,或是其他的商業目的)。
三、 eCTD 文件的編製 (Publishing)
當所有送審文件完成後,申請者也不是就把這些文件一個一個遞交給 FDA,因為在遞交給 FDA 之前,申請者還要先完成 eCTD 文件邊製,英文稱為 Publishing。Publishing 是將申請文件依照 eCTD 的結構與技術規範進行編排、連結與轉換為可提交的電子格式,其目的在於確保如 FDA 等主管機關能有效瀏覽、審查與追蹤申請資料的版本與變更。
四、 數位傳送門:FDA ESG (Electronic Submission Gateway)
當 eCTD 封裝完成後,我們不是透過電子郵件寄給 FDA,而是必須通過 FDA ESG (Electronic Submission Gateway)。
1. 什麼是 Gateway(閘道/門戶)?
ESG 是 FDA 唯一的官方數位收件窗口。它是一個高度加密、自動化的安全傳輸通道,每天處理數以萬計的法規文件。
2. Gateway 的運作邏輯:
- 數位身分證: 申請人(或 U.S. Agent)必須持有 FDA 核可的數位憑證(Digital Certificate)才能登入。
- 自動分流: 當您按下傳送鍵後,Gateway 會辨識文件的案號(IND Number)與收件中心(CDER 或 CBER),自動將文件分發至對應的審查員桌面。
- 回執通知 (Receipts): 送件成功後,Gateway 會回傳關鍵的「電子回執(Receipts)」,證明 FDA 已成功接收並通過行政解密。對 RA 而言,收到這封回執,那 30 天的審查倒數才算正式啟動。
五、 結語:在理性的框架下,呈現科學的溫度
IND 送審文件不只是一堆冰冷的 PDF,它是廠商多年研發心血的總和。身為 RA,我們的價值在於將這些複雜、跨領域的資訊,整理成一套「易於審查」的理性框架。
當我們能讓 FDA 審查員在最短時間內讀懂產品的科學邏輯,並對安全性產生信心時,我們就不只是在遞交文件,而是在為新藥研發的成功率進行「精準導航」。
-------------------------------------------------------------------------------------------------------
職人聲明: 本文內容係基於 FDA 現行 Guidance 及個人實務經驗彙整。內容僅供學術交流參考,不代表官方意見。























