YT: https://youtu.be/vOWUj00_nfI
法說PDF: https://mopsov.twse.com.tw/nas/STR/416920260306M001.pdf
法說影音: https://www.youtube.com/watch?v=M2iTS4WEXhM
泰宗(4169)透過通路銷售與新藥研發雙軌並進,維持穩定獲利並支撐研發投入。U101新藥具備非抗生素機轉,臨床效果顯著,將申請美國三期試驗並拓展全球授權。肝癌檢測平台已取得LDTs認證並開始商轉。未來聚焦高毛利自費市場與國際化布局,長期成長動能明確。

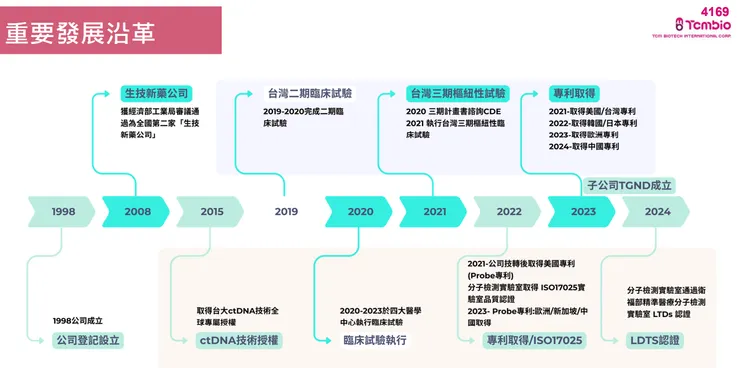
1. 營運亮點概覽 泰宗生物科技(股票代號 4169)深耕醫藥產業數十年,具備代理醫療藥品、先進醫材與新藥研發之能力,是台灣少數兼具通路銷售獲利能力且能穩定成長的新藥研發公司。
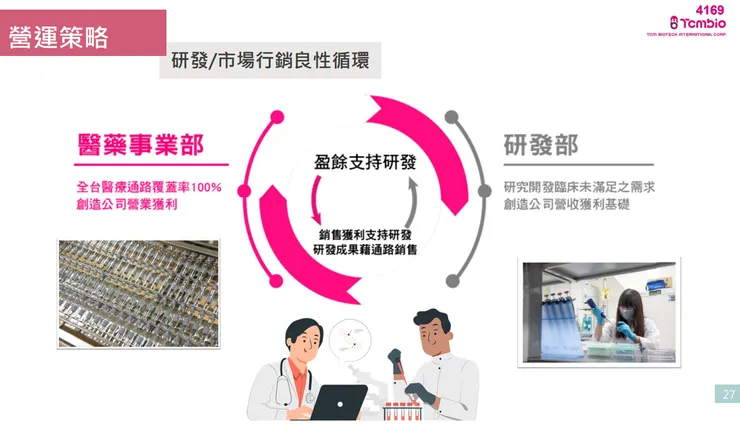
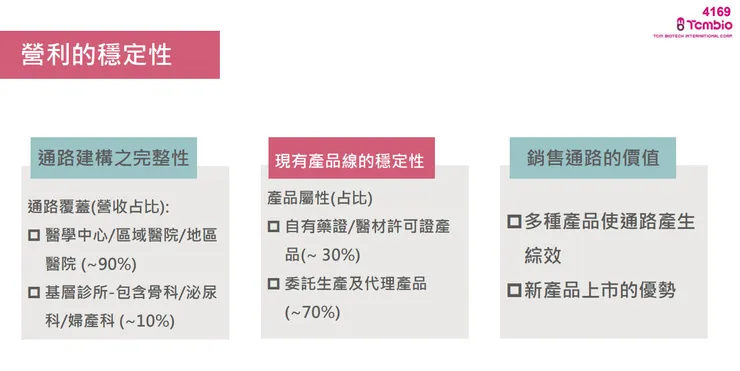
- 營運與研發雙軌並進: 公司採取「研發 + 商業化」的整合優勢,以穩定之自有產品(佔比約30%)與委託生產及代理產品(佔比約70%)的銷售獲利,來支持長期新藥開發(盈餘支持研發),形成良性的研發與市場行銷循環。
- 強大通路優勢: 泰宗在台灣建立極高的醫療通路覆蓋率,醫學中心、區域醫院及地區醫院覆蓋率高達九成(~90%),在基層診所(如骨科、泌尿科、婦產科)也達七成左右,能快速推廣新產品。
- 專業公司治理與團隊: 董事會強調專業治理,多位獨立董事與董事未持有公司股份,藉由外部專家協助公司營運;並設有科技顧問團,以國際前瞻視野定期指導研發方向並評估專案競爭力,降低開發失敗風險。
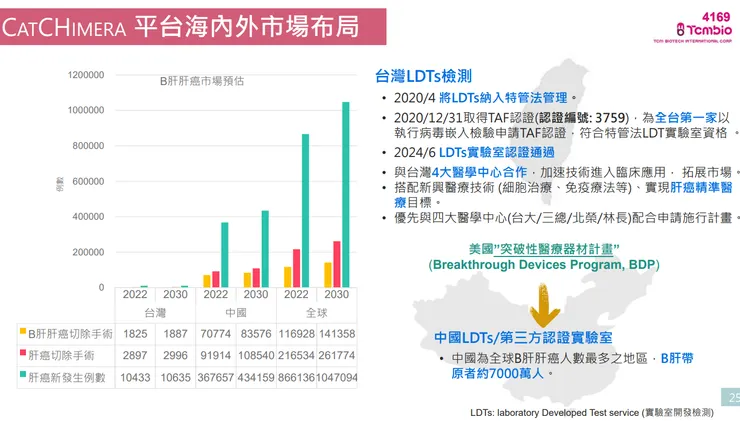
- 檢測服務商轉: CatCHimera 肝癌檢測平台所屬之分子檢測實驗室,已於 2024 年取得台灣衛福部 LDTs(實驗室開發檢測)認證,可正式提供收費服務。
2. 財務業績回顧(QoQ/YoY) 泰宗採取穩健的財務營運模式,以充沛的現金流支持龐大的研發支出。
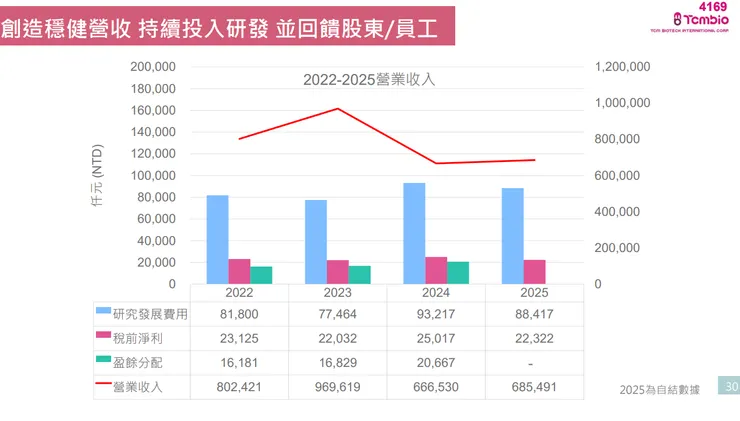
- 營業收入: 2022年為 802,421 千元,2023年達 969,619 千元,2024年為 666,530 千元,2025年(自結)為 685,491 千元。近兩年營收呈現相對下降,主因是因應健保藥價調降,公司策略性放棄部分品項,主動轉向高毛利、高淨利的自費產品發展,未來營收將趨於穩定。
- 稅前淨利: 2022年為 23,125 千元,2023年為 22,032 千元,2024年為 25,017 千元,2025年(自結)為 22,322 千元,獲利表現維持穩定。
- 研究發展費用: 研發投入持續維持高檔,2022年為 81,800 千元,2023年為 77,464 千元,2024年為 93,217 千元,2025年為 88,417 千元。
- 盈餘分配: 公司過去幾年均穩定配發股利(2022年發放 16,181 千元、2023年 16,829 千元、2024年 20,667 千元),113年度(2024年)董事會已核准每股發放現金股利 0.35 元。
3. 未來展望與策略
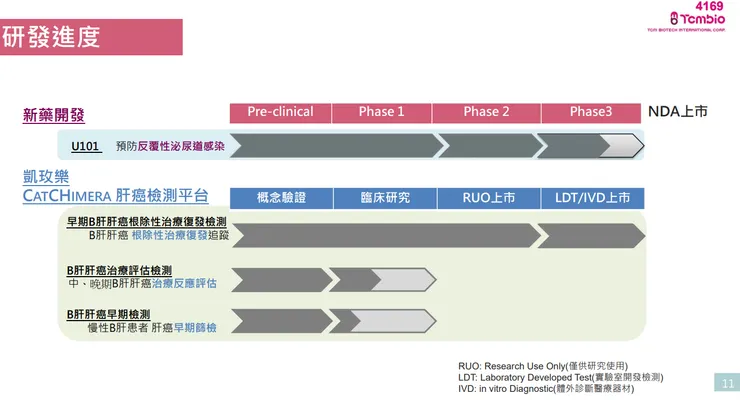
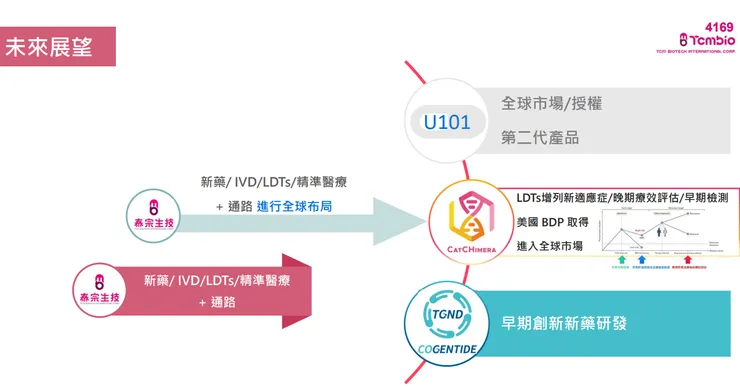
- U101 國際化佈局: 預計今年完成 API(原料藥)的 DMF 準備後,將向美國 FDA 提交三期臨床(IND)申請。美國 FDA 已明確同意 U101 可透過 505(b)(2) 新適應症新藥途徑進入美國三期臨床,並可接受台灣的三期臨床數據作為其樞紐性臨床試驗之一,大幅降低開發成本與時間。此外,公司也將同步啟動歐洲與中國市場的授權與溝通。
- 第二代產品開發: U101 將進行 API 改質與緩釋劑型開發,期望將目前一日服用 2-3 顆的劑型,改良為一日一顆甚至三日一顆,以提升病患服藥便利性。
- CatCHimera 擴大應用與國際認證: 將積極申請美國突破性醫療器材計畫 (BDP) 認證以進軍全球市場,並在台灣 LDTs 規劃增列新適應症、應用於晚期肝癌療效評估及早期肝癌檢測。
- 創新核酸新藥開發: 透過 100% 持股子公司台灣基因核酸新藥 (TGND) 投入早期創新核酸新藥及基因修正新藥之研發,維持公司長期前瞻性。
4. 專題報告(新業務/技術)
A. U101 預防反覆性泌尿道感染 (rUTI) 新藥
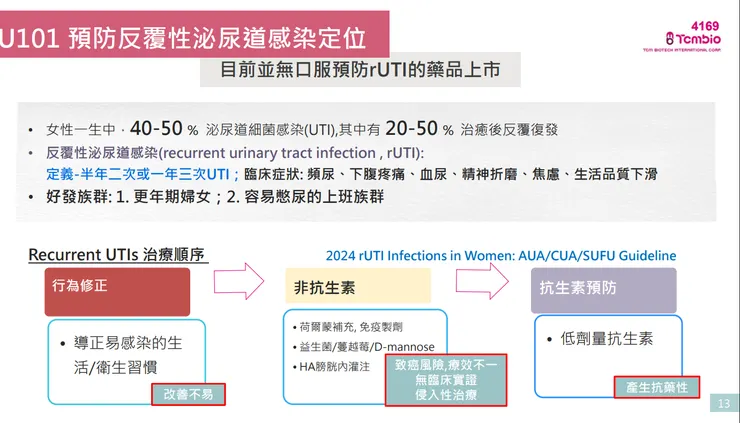
- 未滿足之醫療需求: 40-50% 女性一生中會經歷泌尿道感染,其中 20-50% 治癒後會反覆復發(常見於更年期婦女及憋尿族群)。現行標準治療多依賴長期使用抗生素,容易產生抗藥性問題。
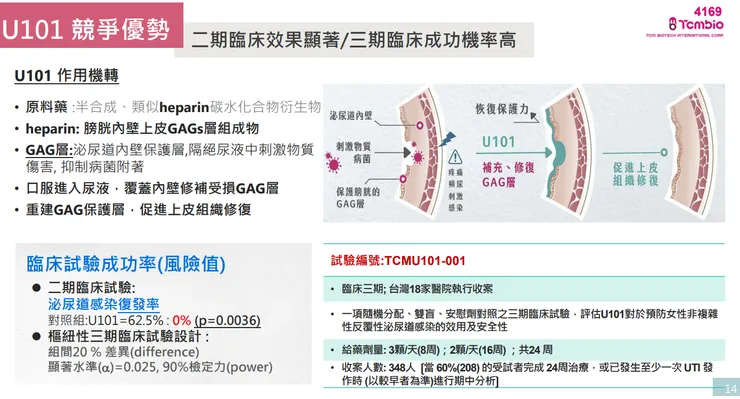
- 創新機轉: U101 為非抗生素療法。其口服後可進入尿液,覆蓋並修復泌尿道內壁受損的 GAG 保護層(類似不沾鍋塗層的防護機制),從根本上隔離尿液刺激物並抑制病菌附著,不會產生抗藥性。
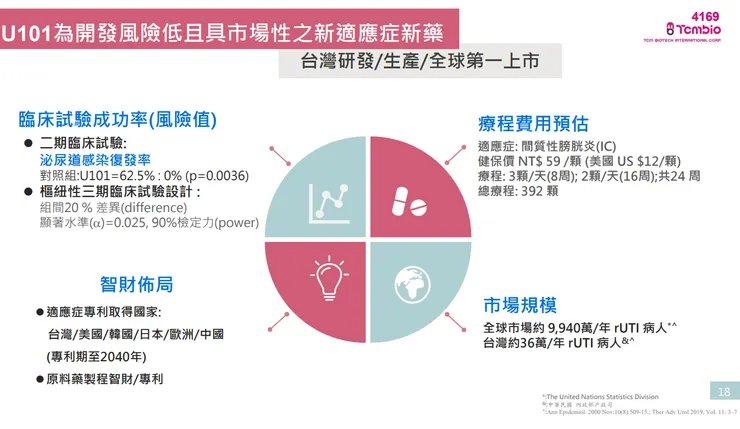
- 臨床與專利進展: 台灣二期臨床結果顯示,對照組復發率高達 62.5%,而 U101 組復發率為 0% (p=0.0036),效果顯著。目前正進行台灣三期臨床試驗(預計收案 348 人),已於去年 11 月達成 60% 收案並啟動期中分析。同時,公司已取得全球適應症專利(保護期至 2040 年),並成功自主開發難度極高的 API,確保未來全球供應與成本優勢。
- 市場規模: 全球約有 9,940 萬名 rUTI 病患,台灣則約有 36 萬名嚴重患者;一個療程長達 6 個月(需服用 392 顆),市場規模極具爆發力。
B. CatCHimera 凱玫樂(B肝肝癌檢測平台)
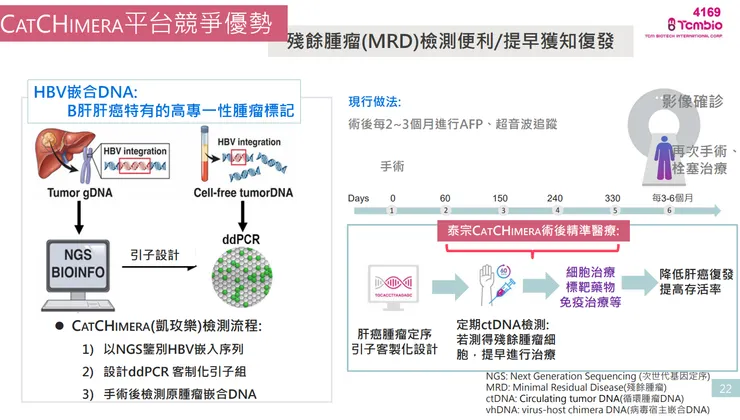
- 未滿足之醫療需求: 早期 B 肝肝癌接受根除性治療(如手術、電燒)後,復發率仍高達 60-70%,且多發生在術後一年內(殘餘腫瘤 MRD 導致),早期復發會大幅降低病患存活率。現有甲胎蛋白 (AFP) 或醫學影像等檢測工具靈敏度與專一性不足,難以早期發現殘存腫瘤。
- 核心技術: CatCHimera 利用 B 肝病毒 (HBV) DNA 隨機嵌合至人體肝細胞 DNA 的獨特嵌合點作為專屬生物標記。透過次世代基因定序 (NGS) 找出專屬序列後,再客製化設計引子,以微滴式數位 PCR (ddPCR) 進行血液檢測。此法可高精準度地追蹤殘餘腫瘤細胞,陽性預測率達 80%,陰性預測率達 92%。
5. 問答環節(Q&A)
- Q1: U101 的作用機轉相較於抗生素與蔓越莓有何優勢? 回答: 研發長表示,U101 不以殺死細菌為目的,而是透過口服在泌尿道黏膜形成類似「不沾鍋」的保護層,使病菌無法附著而隨尿液排出,因此不會產生抗藥性(優於抗生素)。此外,U101 能協助上皮組織修復,停藥後仍能保持預防復發的功用(優於蔓越莓),且口服方式比玻尿酸灌注更安全無侵入性。
- Q2: 公司的股利發放政策與未來配息計畫? 回答: 財務主管說明,政策兼顧股東回饋與長期研發資金需求。依章程規定,股東紅利不低於當年度稅後淨利(扣除 10% 法定公積後)的 50%,現金股利不低於總發放股利的 10%。113年度已核准配發每股現金 0.35 元,未來將繼續秉持此原則。
- Q3: U101 上市後的海內外業務擴展與行銷規劃? 回答: 醫藥事業部副總表示,海外將交由熟悉當地市場的國際夥伴進行授權合作;國內方面,由於目前參與三期臨床的 18 家醫院(含 13 家醫學中心)將作為種子醫院,產品上市後可免除進藥程序 (listing trial) 快速轉換為臨床用藥。加上泰宗既有強大的業務通路,預計上市 6 到 9 個月內即可完成國內 80% 的市場佈局。
- Q4: U101 在美國的佈局進度及原料藥 (API) 供應穩定度? 回答: 總經理回應,已完成美國 FDA 的三期臨床前諮詢 (pre-Phase 3),FDA 同意循 505(b)(2) 途徑並接受台灣三期臨床作為樞紐數據,這將省下龐大研發經費。送出 API DMF 後,預計今年 Q3 申請美國三期臨床。此外,U101 的 API 生產門檻極高,公司耗時 5 年已成功自主掌握量產技術,解決了原廠綁定限制,確保未來進軍全球市場的原料穩定供應。
- Q5: 針對健保連年調降藥價,公司有何具體應對策略?近年營收下降是否與此有關? 回答: 董事長說明,健保調降是長期環境,公司早已佈局,主動放棄部分受影響品項,將資源轉向高毛利、高淨利的自費市場發展,因此造成近兩年營收表面相對下降,但獲利結構轉佳,未來營收將趨於穩定。再者,政府現對生技產業政策趨於友善,新藥上市後將享有約 7 年的專利保護期不被降價,因此獲利空間有充分保障。
免責聲明 (Disclaimer)
本文章/資料之內容僅供參考,不構成任何形式之投資建議、要約、招攬或勸誘。
文中所述之財務數據、營運狀況、預測及產業展望,皆基於公司法說會之口述內容或特定時間點之公開資訊整理而成。未來實際發展可能因總體經濟、產業環境、市場競爭等各種客觀因素變動,而與本文內容或預期有所差異。
本資料可能包含由人工智慧(AI)輔助生成或轉錄之內容,雖已力求語意通順與資訊客觀,但無法保證其完整性與絕對正確性,亦可能存在解讀上的誤差,所有數據與營運資訊應以該公司於「公開資訊觀測站」發布之正式公告為準。
投資一定有風險,金融市場具備波動性。閱聽人及投資者於進行任何投資決策前,應自行獨立判斷、審慎評估相關風險,並自負盈虧。對於任何因直接或間接使用本文資訊而造成之財務損失,本文作者、發布平台及相關資訊提供者概不負責。



















