根據中央健保署最新公布的 2025 年數據,台灣癌症醫療支出創下歷史新高,其中最令人警惕的是:被稱為「癌王」的胰臟癌,十年來首度擠進了十大燒錢癌症榜單 ``。
儘管每年耗費鉅額醫療資源,但胰臟癌的五年存活率依然停滯在令人沮喪的 13% 左右 `。許多人不禁想問:現代醫學這麼發達,各種昂貴的新藥不斷問世,為什麼一旦遇上胰臟癌,往往還是無力回天?
我們到底在對抗一個什麼樣的怪物?最近,國際頂尖科學家終於為我們解開了這個致命謎團。

🛡️ 國際最新發現:癌王自帶打不穿的「隱形防護罩」
就在 2026 年 5 月 1 日,愛爾蘭都柏林三一學院(Trinity College Dublin)的研究團隊在國際權威期刊《Cancer Letters》上發表了一項重大突破,為全球醫界繪製了一份史無前例的「胰臟癌作戰手冊(Battle Manual)」 。
這份作戰手冊揭露了一個殘酷的真相:胰臟癌之所以這麼難治,不只是因為癌細胞極具侵略性,更是因為它非常懂得「築牆防禦」。
科學家發現,在胰臟腫瘤的周圍微環境(Tumor Microenvironment)中,充滿了極度緻密的纖維組織與會抑制免疫力的細胞 。這就像是癌細胞為自己打造了一座「鋼筋水泥的防空洞」。這層厚重的物理與生物防護罩,不僅會把昂貴的抗癌標靶藥物與化療死死擋在外面,還會直接癱瘓人體免疫系統的攻擊,讓癌細胞在裡面肆無忌憚地壯大 。
這篇文章是一篇發表於 2026 年《Cancer Letters》期刊上的回顧性文獻,標題為「胰臟癌的特徵(The hallmarks of pancreatic cancer)」。文章主要將著名的「癌症特徵(Hallmarks of Cancer)」理論應用於胰臟癌(Pancreatic Cancer, PC)的具體情境中,探討其獨特的致病機制與微環境。
以下是文章的重點摘要:
1. 核心背景與挑戰
- 全球預後最差的癌症:胰臟癌的 5 年存活率僅約 13%,主要是因為發現時往往已是晚期、腫瘤微環境(TME)具高度侵襲性,且治療選擇有限。
- 癌症特徵的演進:定義惡性腫瘤的「癌症特徵」在過去 25 年間不斷擴充,從最初的 6 項發展至今已達 14 項。本文旨在探討這 14 項特徵在胰臟癌中的具體表現機制,以促進更有價值的未來研究。
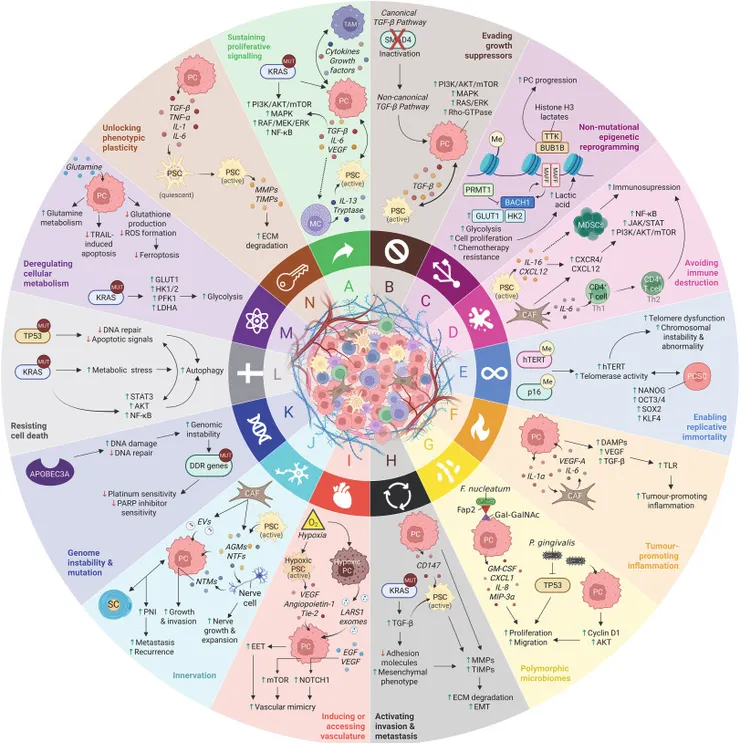
圖片來源:https://www.sciencedirect.com/science/article/pii/S0304383526002004?via%3Dihub
- (A) 持續的增殖訊號 (Sustaining proliferative signalling)
- (B) 規避生長抑制因子 (Evading growth suppressors)
- (C) 非突變性的表觀遺傳重編程 (Non-mutational epigenetic reprogramming)
- (D) 避免免疫破壞 (Avoiding immune destruction)
- (E) 啟動複製永生性 (Enabling replicative immortality)
- (F) 促癌炎症 (Tumour-promoting inflammation)
- (G) 多樣化的微生物群 (Polymorphic microbiomes)
- (H) 啟動侵襲與轉移 (Activating invasion and metastasis)
- (I) 誘導或獲取血管系統 (Inducing or accessing vasculature)
- (J) 神經支配 (Innervation)
- (K) 基因組不穩定性與突變 (Genome instability and mutation)
- (L) 抵抗細胞死亡 (Resisting cell death)
- (M) 細胞代謝失調 (Deregulating cellular metabolism)
- (N) 解鎖表型塑性 (Unlocking phenotypic plasticity)
2. 胰臟癌的腫瘤微環境(TME)與進展
- 基因突變與異質性:胰臟癌(尤其是佔 85-90% 的胰臟導管腺癌 PDAC)的進展通常伴隨 KRAS 和 TP53 等關鍵基因的驅動突變。研究發現腫瘤內部存在極大的空間與基因異質性。
- 結締組織增生(Desmoplasia):這是胰臟癌最顯著的特徵之一。腫瘤周圍會形成緻密的基質(可佔腫瘤體積的 80%),導致微環境缺氧、缺乏營養,且在免疫上呈現「冷(Cold)」的狀態(缺乏免疫細胞浸潤)。
- 關鍵細胞:胰臟星狀細胞(PSCs)和癌症相關纖維母細胞(CAFs)是產生這些緻密膠原基質的關鍵,它們與癌細胞有雙向的交互作用,會促進腫瘤存活、增殖甚至轉移。
3. 治療困境與反思
- 基質標靶治療的挫折:由於緻密的基質會阻礙化療藥物進入腫瘤,科學家曾嘗試針對基質細胞(如消除 CAFs)進行標靶治療。然而,臨床前與臨床數據顯示結果令人失望;極度消除基質反而可能導致腫瘤變得更具侵襲性、增加轉移能力,甚至導致患者存活率下降。
- 精準醫療的需求:儘管目前有針對胰臟癌分子亞型的分類嘗試(如 PurIST 模型)以提供個人化治療,但仍受限於活檢樣本小、缺乏統一標準以及可行的標靶突變過少等問題。
總結來說,這篇文獻詳細梳理了胰臟癌如何利用其獨特的基因突變與緻密的腫瘤微環境來維持其惡性特徵。作者強調,深入理解這些專屬於胰臟癌的運作機制,對於未來開發早期檢測生物標記與新型治療策略(如更精準地重塑腫瘤微環境而非單純消除它)至關重要。
這就是為什麼,等到晚期出現症狀才開始吃藥治療,往往已經太遲,因為武器根本打不進去!
⏳ 唯一的保命解方:在「防空洞」建好前,提早引爆它
看懂了癌王的防禦機制,我們就能找到破解的戰略。這份作戰手冊強烈呼籲:既然晚期的防護罩打不穿,我們未來的唯一勝算,就是「極早期的精準診斷」 ``。
必須在腫瘤還極度微小、防護罩還沒完全成型之前,就把它揪出來切除!
但這也是醫學界長期以來的最大痛點。早期的胰臟腫瘤通常小於 2 公分,在傳統的腹部電腦斷層(CT)掃描上,就像水中的一滴淡墨般模糊。
從真實的臨床現場來看,這簡直是一場「隱形捉迷藏」。有時,即使是經驗豐富的放射科醫師,也可能受限於人類視覺的極限,將早期的微小異常誤判為良性的囊腫(例如常見的 IPMN)。這導致大約有 40% 的早期病灶會在肉眼判讀時被遺漏,讓病患白白錯失了逃生門。
🏥 避險投資:用「有執照的 AI」升級你的健康防護網
面對如此狡猾的敵人,我們不能只靠人類肉眼的極限。但請注意,我們需要的絕不是網路上那種會產生「幻覺」、甚至引發嚴重醫療決策風險(正如國際 ECRI 報告所強烈警告的)的聊天機器人,而是需要真正取得官方認證的「醫療級 AI(SaMD)」。
幸運的是,在台灣,我們已經擁有了領先全球的防禦武器:由台灣本土團隊研發的 AI 輔助診斷系統——「助胰見(PANCREASaver)」。
它不僅取得了台灣 TFDA 醫材許可,更榮獲了美國 FDA「突破性醫材」的雙重最高肯定。這套系統就像一雙不會疲累的顯微電眼,能全自動深度分析 CT 影像。在真實的臨床實戰中,它甚至能敏銳地在醫師認為「只是良性囊腫」的影像中,精準揪出隱藏的惡性胰臟癌,扮演了最關鍵的救命吹哨者。
醫學數據證實,只要能靠著這套 AI 系統,在腫瘤「小於 2 公分」時及早發現,胰臟癌的存活率就能從晚期的不到 10%,戲劇性地狂飆至 80%!
🎯 結語:主動出擊,別讓健檢做白工
面對這場與癌王的生死博弈,最聰明的健康資產配置,絕對不是存錢等著未來買天價的新藥,而是現在就為自己安排具備「AI 輔助判讀」的高階自費健檢。
與其跟打不穿的防護罩硬碰硬,不如善用尖端科技提早排雷。下一次安排健康檢查時,請務必主動指名使用「助胰見」等醫療級 AI 來為您把關。主動掌握極早期發現的黃金契機,才是現代人最極致、最務實的保命之道!






















