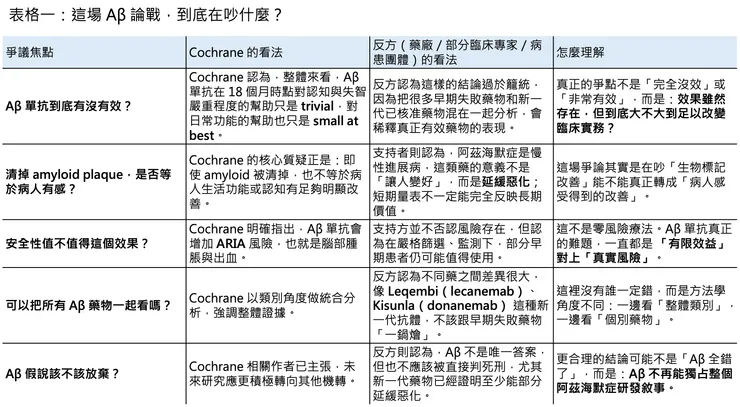
4 月 16 日,一篇來自 Cochrane 的系統性綜述,再次把阿茲海默症領域最核心、也最具爭議的主軸,推回風暴中心。這份綜述的訊息極其刺耳:對輕度認知障礙(MCI)或輕度失智的阿茲海默症患者而言,amyloid-beta targeting monoclonal antibodies 在 18 個月時點對認知功能與失智嚴重程度的改善只是 trivial,對日常功能的幫助也僅是 small at best;相對地,卻會增加 amyloid-related imaging abnormalities(ARIA),也就是腦部腫脹與微小出血的風險。更直接地說,就算這些藥真的把腦中的 amyloid 清掉了,患者未必能換到足夠有感的臨床利益。
真正讓這場爭論瞬間升溫的,不只是 Cochrane 的語氣夠重,而是它碰到的是一條已經不只是學術假說,而是產業事實的路線。Aβ 假說自 1991 年被提出後,幾乎形塑了整個阿茲海默症新藥研發的方向;直到今天,它仍是已核准疾病修飾療法背後最核心的生物學邏輯之一。換句話說,這不是一場純學院內部的機制辯論,而是一場牽動監管、資本、支付、臨床與病人期待的全面對撞。
/ 01 /為什麼這份報告像一份「宣判書」?
因為它挑戰的,正是過去二十多年來整個領域最核心的信念:清除 amyloid plaque,是否真的能改變阿茲海默症的病程? Cochrane 的答案很接近「不夠」。它並不是否認所有藥物都沒有任何統計學差異,而是指出,從整體證據來看,這些差異在 18 個月的觀察時點,還不足以構成大多數患者能真切感受到的臨床改變。這裡的關鍵詞不是 “no effect”,而是 “no clinically meaningful effect”。也就是說,問題不在於量表上有沒有變化,而在於這種變化,是否足以改變病人和家屬的真實生活。
這個結論之所以刺耳,是因為 anti-amyloid 單抗並不是沒有代價。Cochrane 明白指出,這類藥物會提高 ARIA 的風險,包括腦水腫與微出血。從藥理學上看,這並不令人意外:當你快速、大量地移除腦內 amyloid,血管與腦組織就可能付出代價。問題在於,如果藥物帶來的是 MRI 上看得見、患者卻不一定換得到足夠實質利益的風險,那整個風險效益比就會被重新檢視。這也是為什麼這篇綜述一出,許多人會把它解讀成對 Aβ 假說的一記重錘。
/ 02 /但這不是故事的全部:為什麼藥廠、臨床醫師與病患團體立刻反擊?
因為 Cochrane 的做法,碰到了一個 anti-amyloid 領域最敏感的爭點:能不能把不同世代、不同強度、不同失敗原因的藥,全部打包成一個「類別結論」? Alzheimer’s Research UK 很快就指出,這份綜述雖然納入了 lecanemab 與 donanemab,但相當大一部分證據其實來自較早期、後來已被放棄的失敗藥物。換句話說,反方的核心意見不是說 Cochrane 造假,而是說它把「舊世代低效或失敗的 anti-amyloid 藥」和「已經在第三期試驗中打出統計學顯著結果、並完成監管核准的新藥」混在一起分析,最後得到一個對整個類別都過於悲觀的印象。
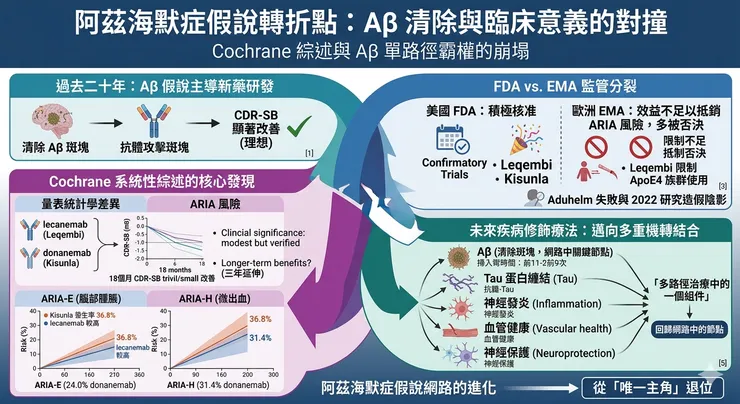
這個反擊之所以站得住腳,是因為 lecanemab 和 donanemab 的確不是空手而來。Leqembi(lecanemab) 在 Clarity AD 試驗中,18 個月時於 CDR-SB 的調整後差值為 -0.45,相當於 27% 的臨床惡化減緩;FDA 也因此在 2023 年將它從加速核准轉為傳統完全核准,並明言 confirmatory trial 已驗證臨床利益。Kisunla(donanemab) 則在 TRAILBLAZER-ALZ 2 中,於 76 週在 iADRS 與 CDR-SB 都達到統計顯著差異,FDA 於 2024 年核准用於 MCI 或輕度失智階段的阿茲海默症。也就是說,若把問題換成「這兩款新世代藥物是否完全沒有效果」,答案其實不是。
但另一邊也不能假裝安全性不是問題。以 donanemab 為例,在 JAMA 發表的 TRAILBLAZER-ALZ 2 中,任何 ARIA 的發生率為 36.8% vs 14.9%,其中 ARIA-E 為 24.0% vs 2.1%,ARIA-H 為 31.4% vs 13.6%。這正是 anti-amyloid 支持者最難迴避的現實:你可以主張這些藥不是沒效,但你很難再說它們是「乾淨而輕鬆」的治療。也因此,今天真正的爭論其實不是「有沒有效」這麼二分,而是:這種效果,到底值不值得用這樣的風險與醫療資源去換?
更複雜的是,「臨床意義」本身就不是一個全世界已有共識答案的詞。Alzheimer’s Research UK 直接指出,目前其實並沒有 universally agreed definition 來界定什麼才叫 clinically meaningful;而對家屬來說,哪怕只是多爭取幾個月相對穩定、能保持自主性的時間,都可能非常重要。也就是說,Cochrane 抓到的是一個很硬的實證醫學問題,但反方抓到的,則是一個同樣真實的臨床與照護問題。這兩種語言,不一定會自然對齊。
/ 03 /其實,Aβ 路線的信任危機,早就不是今天才開始
如果今天的爭議只來自 Cochrane,那這場風暴不會這麼大。真正的背景是:Aβ 這條路線在過去幾年,已經歷經了太多折返、太多創傷,也太多讓外界難以忘記的事件。
最具代表性的,當然還是 Aduhelm(aducanumab)。這款藥在 2021 年獲 FDA 加速核准時,就因臨床證據爭議而掀起巨大風暴;當年 FDA 諮詢委員會對其效益採取近乎一面倒的反對態度,之後更引發多名委員辭職。到了 2024 年 1 月,Biogen 宣布停止 Aduhelm 的開發與商業化,並終止 ENVISION confirmatory study,將資源轉往 Leqembi 與其他 tau 相關資產。公司雖強調此決定「不是基於安全性或有效性疑慮」,但在產業敘事上,Aduhelm 幾乎已成為 Aβ 路線最深的一道裂痕。
另一層更深的陰影,則來自基礎研究信任本身。2022 年開始,2006 年一篇聚焦 Aβ*56 的知名研究,因影像操弄與數據可靠性問題遭到嚴重質疑,之後更走向撤稿程序。這起事件無疑重傷了外界對 amyloid 領域部分基礎文獻的信心,但它也沒有徹底摧毀整個 Aβ 假說。包括 Alzheimer’s Society 在內的多方都強調,Aβ*56 只是 amyloid 生物學裡很小的一塊,並不等於整個 amyloid 與 Alzheimer’s disease 的關聯都被推翻。 這也是今天這場論戰最容易被簡化、卻最不能被簡化的地方:Aβ 研究有過度延伸、也有誤判與醜聞,但這不代表所有 amyloid biology 都是錯的。
/ 04 /真正的分水嶺,其實寫在監管端:FDA 與歐洲看的是同一份資料,卻做出不同判斷
如果 anti-amyloid 的證據真的那麼清楚,今天全球監管不會出現這麼分裂的畫面。
美國 FDA 的立場相對積極。它先在 2023 年給了 Leqembi(lecanemab) 傳統完全核准,並明確表示 confirmatory trial 已驗證臨床利益;接著又在 2024 年核准 Kisunla(donanemab)。從 FDA 的語氣來看,它接受的核心邏輯是:對早期阿茲海默症患者而言,這類藥物雖不是逆轉疾病,但已足以被視為首批真正 touching the underlying disease process 的療法。
但歐洲的態度明顯更保守。Leqembi 在 2024 年 7 月先被 CHMP 否決,理由正是「延緩退化的幅度不足以抵銷嚴重腦水腫風險」;直到 re-examination 後,EMA 才於 2024 年 11 月改為支持在限制族群中使用,也就是僅限 ApoE4 只有 0 或 1 個拷貝、且有 amyloid beta plaque 的早期患者,歐盟執委會並於 2025 年 4 月正式核准。相較之下,Kisunla(donanemab) 到了 2025 年 3 月仍遭 EMA 拒絕,理由同樣是效益不足以抵銷嚴重腦腫脹風險。這說明了一件很現實的事:同一份科學證據,在不同監管文化與風險容忍度下,可能得到完全不同的政策答案。

這也讓今天的爭議更像是一場「效益到底要大到什麼程度,才算足以改變臨床實務」的戰爭,而不只是單純的機制之爭。FDA 願意為 modest but verified benefit 開一扇門;歐洲則更強調風險效益比,且把安全族群切得更窄。對藥廠來說,這意味著 anti-amyloid 已不再是只要把 plaque 清乾淨就夠,而是必須同時回答:哪些患者最可能受益、哪些患者風險最高、何時介入才最合理。
/ 05 /所以,Aβ 假說該被放棄嗎?
我會說,Aβ 作為阿茲海默症唯一主線的時代,確實已經結束;但 Aβ 作為疾病網路中的一個關鍵節點,還沒有被判死刑。
這正是今天這場爭論最應該留下來的結論。Cochrane 把過去產業不願正視的問題,直接攤在陽光下:把 amyloid 清掉,不等於自動換來足夠大的臨床利益;而 anti-amyloid drugs 帶來的風險、監測負擔與成本,也不能再被「終於有藥了」這種情緒掩蓋。這是一記必要的重錘。
但若因此直接宣告「Aβ 假說已死」,也同樣過頭。因為今天至少已經有 lecanemab 與 donanemab 這兩款藥,在嚴格篩選的早期患者中證明了疾病進程可以被拉慢;支持者也提出,18 個月可能仍太短,較長期的延伸追蹤或真實世界資料,或許更能看出這類 disease-modifying therapy 的累積效果。Eisai 在 2024 年公布的延伸資料就主張,lecanemab 連續三年治療後,CDR-SB 的分離幅度持續擴大;Alzheimer’s Research UK 也明言,較長期證據可能顯示 modest but sustained benefits,而這些新資料並未完整反映在 Cochrane 的分析裡。這些主張未必已經蓋棺定論,但至少說明,anti-amyloid 的故事還沒講完。
更重要的是,整個領域其實早就已經往「Aβ 不是全部答案」的方向移動。Alzheimer’s Society 早在討論 Aβ*56 爭議時就說得很清楚:現在大家愈來愈相信,真正驅動阿茲海默症的,不只是 amyloid,還包括 tau、inflammation、blood vessel health 等多重機制。也就是說,未來最有可能成功的,不會是一顆單純把 amyloid 清掉的 magic bullet,而更可能是更早期介入、做更準的病人分型,甚至把 anti-amyloid 與 anti-tau、抗發炎或神經保護策略結合。這不代表 Aβ 白做了,而是代表它必須從「唯一主角」退位成「多路徑治療中的一個組件」。
阿茲海默症研發從來就不是一條直線。今天 Cochrane 的這份報告,不是最終判決,而是一次強迫全產業重新誠實面對證據的時刻。它逼著支持者承認:清 plaque 不是萬靈丹;也逼著反對者承認:至少有些新一代 anti-amyloid drugs,確實已經把「完全無法改變病程」這個舊認知往前推了一步。真正崩塌的,也許不是 Aβ 本身,而是那種信仰式、單一路徑式的 Aβ 霸權。接下來十年,阿茲海默症領域最需要的,恐怕不再是「要不要相信 Aβ」,而是怎麼把 Aβ 放回它真正該在的位置上。
------------
參考資料:
[0]:公開資料&各公司官網
[1]: https://www.cochrane.org/evidence/CD016297_are-medicines-anti-amyloid-monoclonal-antibodies-reduce-build-abnormal-proteins-brain-effective "Are medicines (anti-amyloid monoclonal antibodies) that reduce the build-up of abnormal proteins in the brain an effective treatment for people with mild cognitive impairment or mild dementia due to Alzheimer’s disease, and do they cause unwanted effects? | Cochrane"
[2]: https://www.alzheimers.org.uk/what-we-do/researchers/news/explaining-amyloid-research-study-controversy "Explaining the amyloid research study controversy | Alzheimer's Society"
[3]: https://www.alzheimersresearchuk.org/news/leaders-in-the-field-react-to-study-with-major-limitations-labelling-alzheimers-drugs-as-ineffective/ "Leaders in the dementia field react to a report with ‘major limitations’ labelling Alzheimer’s drugs as ineffective - Alzheimer's Research UK"
[4]: https://www.eisai.com/news/2024/news202456.html "New Clinical Data Demonstrates Three Years of Continuous Treatment with Dual-Acting LEQEMBI® (lecanemab-irmb) Continues to Significantly Benefit Early Alzheimer’s Disease Patients Presented at AAIC 2024 | News ReleaseNews Release:2024 | Eisai Co., Ltd."
[5]: https://jamanetwork.com/journals/jama/fullarticle/2807533 "Donanemab in Early Symptomatic Alzheimer Disease: The TRAILBLAZER-ALZ 2 Randomized Clinical Trial | Trials | JAMA | JAMA Network"






















