【嬌生 CAR-T 戰略折戟:不是數據不夠漂亮,而是自體 CD19/CD20 CAR-T 的商業死循環開始反噬】
📌 誰能想到,幾個月前還被 Johnson & Johnson 管理層高度看好的淋巴瘤 CAR-T 管線,會在 2026 年 4 月底被突然送進歷史檔案夾。這不是普通的管線微調。
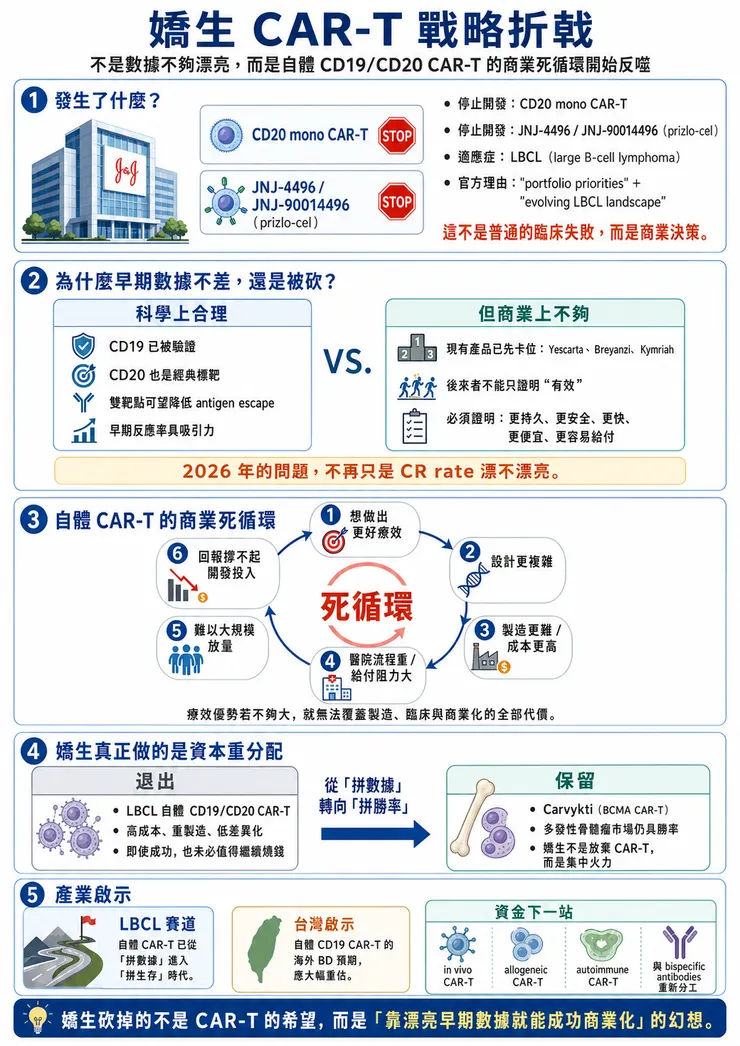
Johnson & Johnson 宣布停止開發兩款 large B-cell lymphoma(LBCL)CAR-T 療法:一款是 CD20 mono CAR-T,另一款是 CD19/CD20 bi-CAR-T,也就是外界熟知的 JNJ-4496 / JNJ-90014496(prizloncabtagene autoleucel, prizlo-cel)。公司給出的官方理由很克制:這是基於「portfolio priorities」以及對「evolving large B-cell lymphoma treatment landscape」的評估所做出的策略性商業決策。換句話說,這不是單純臨床失敗,而是強生判斷這條賽道即使成功,也未必值得繼續燒錢。
這件事真正震撼的地方在於:JNJ-4496 不是一條毫無數據的管線。
2025 年 6 月,Johnson & Johnson 才在 EHA 發表 JNJ-4496 的 Phase 1b 數據,將它描述為一款 dual-targeting anti-CD19/CD20 bispecific autologous CAR-T,用於 relapsed / refractory large B-cell lymphoma。當時資料釋放出的訊號相當漂亮,也讓外界一度認為它有機會成為下一代淋巴瘤 CAR-T 的核心競爭者。
然而不到一年,嬌生選擇全線停手。這代表什麼?自體 CD19/CD20 淋巴瘤 CAR-T 的商業模式進入最殘酷的下半場。過去大家只問一個問題:你的 CR rate 夠不夠高?
現在大藥廠問的是另一個問題:你的療效優勢,足不足以支付製造成本、臨床開發成本、商業化複雜度、給付阻力,以及未來與既有產品和下一代療法競爭的全部代價?嬌生這次的答案很明確:不值得了。
【01|從「best-in-disease」到被終止:自體 CAR-T 的殘酷落差】
JNJ-4496 的故事,本來非常符合下一代 CAR-T 的敘事模板。
- 🧬 第一,CD19 已經被驗證。
- 🧬 第二,CD20 也是 B-cell lymphoma 的經典標靶。
- 🧬 第三,雙靶點理論上可以降低 antigen escape。
- 🧬 第四,Johnson & Johnson 不是小公司,它有 Carvykti 的商業化與細胞治療經驗。
- 🧬 第五,早期臨床數據看起來確實不差。
這樣的組合,放在 2021 或 2022 年,幾乎會被市場直接貼上「下一個 blockbuster CAR-T」標籤。但 2026 年的市場,已經不是那個市場。
LBCL 的自體 CAR-T 賽道,早就不是藍海。
Yescarta(axicabtagene ciloleucel) 已經在 large B-cell lymphoma 的二線治療建立地位;FDA 早在 2022 年即核准 axicabtagene ciloleucel 用於一線 chemoimmunotherapy 後 12 個月內復發或 refractory 的成人 LBCL。這代表 CD19 CAR-T 已經不是最後線奇兵,而是開始前移到更早治療線。
Breyanzi(lisocabtagene maraleucel) 也持續擴張適應症與使用場景。Kymriah(tisagenlecleucel) 雖然商業表現不如前兩者,但也早已完成第一代市場教育。這些產品共同把 CD19 CAR-T 的療效門檻、醫師認知與給付討論拉到一個很高的位置。
因此,JNJ-4496 就算早期 CR rate 好看,也必須回答一個更難的問題:它到底比現有 CD19 CAR-T 好在哪裡?
是更持久?更安全?更便宜?更快?更容易製造?能門診給藥?能顯著降低 relapse?能直接進二線甚至一線?還是能打出 payer 願意額外付費的清楚差異?如果答案只是「雙靶點、反應率漂亮」,那在今天已經不夠了。

【02|這不是臨床失敗,而是商業模型失敗】
嬌生沒有說這兩條管線因安全性或療效問題被砍。它說的是 portfolio priorities 和 evolving LBCL landscape。這句話很官方,但翻譯成產業語言,就是:這個市場已經捲到投入產出比不划算。
自體 CAR-T 最大的問題,從來不只是科學。它是一個非常重的商業系統。
- 💰 病人要 leukapheresis。
- 💰 細胞要送去製造。
- 💰 製造要等數週。
- 💰 患者可能需要 bridging therapy。
- 💰 產品要回輸。
- 💰 醫院要有細胞治療中心。
- 💰 醫師要管理 CRS、ICANS、感染、血球低下。
- 💰 保險要預先核准。
- 💰 給付要談判。
- 💰 製造失敗與物流風險要吸收。
這一整套系統,決定了自體 CAR-T 很難像小分子或抗體一樣自然放量。更致命的是,LBCL 已經有多個成熟 CAR-T 產品。當一個新產品進場時,不能只證明「我有效」,而是要證明「我值得整個醫療系統重新為我安排流程」。這就是自體 CD19/CD20 CAR-T 的死循環:療效要更好,所以設計更複雜。設計更複雜,製造更難、成本更高。成本更高,就需要更高價格或更大市場。但市場已經有 Yescarta、Breyanzi 等先行者,醫院與 payer 不會輕易給新產品超額溢價。如果無法顯著降低成本或顯著改善臨床結局,商業化回報就撐不起開發投入。嬌生這次砍管線,砍的不是一個藥。它砍的是這個死循環。
【03|雙靶點不是免死金牌】
🎯 JNJ-4496 的設計邏輯很直覺:同時靶向 CD19 與 CD20,希望降低單一抗原逃逸造成的復發。
這個科學邏輯沒有錯。Gilead / Kite 也在做類似方向。Kite 的 KITE-363 與 KITE-753 都是 autologous anti-CD19/CD20 CAR-T,正在 relapsed / refractory B-cell lymphoma 中進行 Phase 1/2 研究。Gilead 的公開臨床試驗資料也明確指出,PALISADES-1 正是在評估 KITE-363 或 KITE-753 的安全性與療效。
所以,嬌生退場不代表 CD19/CD20 雙靶點完全沒戲。
但它代表雙靶點本身已經不是足夠差異化。如果大家都知道 CD19/CD20 可能解決 antigen escape,那麼市場接下來比較的就不是「你是不是雙靶點」,而是:
- 💰 誰製造更穩?
- 💰 誰毒性更低?
- 💰 誰劑量更低?
- 💰 誰能門診?
- 💰 誰能用更少中心推廣?
- 💰 誰能更快從 leukapheresis 到回輸?
- 💰 誰能在真實世界維持和臨床試驗接近的療效?
- 💰 誰能讓 payer 相信多花錢值得?
在這個比較框架下,JNJ-4496 即使數據漂亮,也未必能形成壓倒性優勢。這就是為什麼「科學上合理」和「商業上值得」之間,現在出現了非常大的裂縫。
【04|嬌生不是放棄 CAR-T,而是把籌碼集中到更有勝率的地方】
🧭 要注意,Johnson & Johnson 並沒有完全退出 CAR-T。它仍然有 Carvykti(ciltacabtagene autoleucel)。Carvykti 是 J&J 和 Legend Biotech 合作開發的 BCMA CAR-T,用於 multiple myeloma。它在多發性骨髓瘤市場已經建立非常強的臨床與商業位置。J&J 2026 年第一季財報顯示,公司 Innovative Medicine 業務持續由 oncology 推動成長,Carvykti 也被多家市場觀察者視為其未來重要增長產品之一。
所以強生不是「看空所有 CAR-T」。它是在做更精確的資本配置:多發性骨髓瘤的 BCMA CAR-T,仍然值得打。而高度內卷的 LBCL 自體 CD19/CD20 CAR-T,不值得再花大錢硬拚。這個差別很重要。
大型藥廠現在不是沒有錢,而是更不願意為低差異化產品支付高昂開發成本。尤其在 CAR-T 這種製造與商業化極度複雜的領域,僅僅有漂亮早期數據,已經不足以讓總部一路放行。過去是「有療效就能融資、能授權、能講 blockbuster」。現在是「有療效之後,還要證明你有可放大的商業化路徑」。這就是後疫情時代 CGT 投資邏輯最大的變化。
【05|LBCL 自體 CAR-T 正在從「拼數據」變成「拼生存」】
LBCL CAR-T 的競爭正在進入一個更殘酷的階段。早期時代,CD19 CAR-T 是革命性療法。只要能讓 refractory lymphoma 患者達到深度緩解,就足以震撼市場。但現在,標準變了。
醫師已經知道 CAR-T 會有效。患者也知道 CAR-T 是一種選擇。醫院也已經建立部分流程。payer 也已經看過這類產品的價格與真實世界成本。因此,後來者必須拿出更硬的東西。不是 20 個病人的 CR 率。不是單臂 Phase 1b 的漂亮 waterfall plot。不是「可能 best-in-disease」的口號。而是可被 payer、醫院、指南與真實世界醫療系統共同接受的綜合優勢。
這包括:
- ⚖️ 更長的 PFS / OS。
- ⚖️ 更低的 ICU 與住院需求。
- ⚖️ 更低 CRS / ICANS 管理負擔。
- ⚖️ 更短製造週期。
- ⚖️ 更低製造失敗率。
- ⚖️ 更明確的二線或一線定位。
- ⚖️ 更簡單的給付理由。
- ⚖️ 更能與現有 bispecific antibodies、ADC、T-cell engagers 和新型免疫療法區分。
如果這些都沒有,早期數據再漂亮,也可能只是昂貴的科學樣品。嬌生這次退場,就是給整個產業上的一課:CAR-T 不是不能做,而是不能再用 2020 年的故事去融 2026 年的錢。
【06|最該被重估的,是自體 CD19 CAR-T 的BD 大藥廠預期】
這件事說的直接一點:自體 CD19 CAR-T,基本不應該再被賦予明顯大藥廠 BD 預期。
產業格局已經變了。連 Johnson & Johnson 這種等級的藥廠,面對一條早期數據不差、CD19/CD20 雙靶點設計、曾被視為潛在 multi-billion asset 的 LBCL 自體 CAR-T,都選擇因為 portfolio priority 和 evolving landscape 退場,那一般生技公司一個相對小規模、缺乏全球 CAR-T 商業化網絡、缺乏大規模 GMP 製造經驗、缺乏國際多中心註冊性試驗能力的自體 CD19 CAR-T,憑什麼還能期待大藥廠的高價 BD?
大藥廠現在逃離的,不是所有細胞治療。
它們逃離的是這種 高成本、重製造、低差異化、競品成熟、給付困難、放量受限 的自體 CAR-T 死循環賽道。自體 CD19 CAR-T 如果還停留在「我們也有 CD19 CAR-T」、「我們在可以做」、「我們有臨床經驗」這種敘事,大藥廠 BD 幾乎沒有想像空間。因為海外買家不缺 CD19 CAR-T。他們缺的是:能顯著降低製造成本的技術。
- 能縮短 vein-to-vein time 的平台。
- 能做 allogeneic 或 in vivo CAR-T 的底層能力。
- 能在自體免疫疾病中免疫重置的安全方案。
- 能用新遞送技術繞開傳統細胞製造流程的下一代產品。
- 能在特定市場形成真實現金流與病人資料的區域解法。
換句話說,自體 CD19 CAR-T 的合理價值,不應該放在「授權給 MNC」這個故事上。它比較可能的定位,是某些區域型醫療服務、特管或再生醫療制度下的在地治療方案、細胞製備能力、醫院合作網絡,或是作為未來更高階細胞治療技術的製造基礎。這和 BD給大藥廠 是兩回事。
【07|下一代 CAR-T 的錢,正在流向哪裡?】
嬌生砍掉 JNJ-9530 和 JNJ-4496,不代表資本完全離開 CAR-T。它只是從成熟內卷的自體 CD19 LBCL 賽道,轉向更有結構性突破機會的地方。
- 🚀 第一,是 in vivo CAR-T。Eli Lilly 連續收購 Orna Therapeutics 和 Kelonia Therapeutics,就是最清楚的訊號。大藥廠真正想要的,是繞開傳統自體 CAR-T 製造流程,直接在病人體內完成 T cell engineering。這才是顛覆成本結構的路。
- 🚀 第二,是 allogeneic CAR-T。雖然異體 CAR-T 過去一直被持久性、免疫排斥與安全性困擾,但如果能解決這些問題,它的即用型與規模化潛力遠高於自體療法。
- 🚀 第三,是 autoimmune CAR-T / immune reset。SLE、myositis、systemic sclerosis、multiple sclerosis 等自體免疫疾病,正在成為 CAR-T 新敘事。這裡的市場邏輯不是殺腫瘤,而是重置免疫系統。相較高度內卷的 LBCL,這是大藥廠更願意提前卡位的新戰場。
- 🚀 第四,是 CAR-T 與 bispecific antibodies 的重新分工。在某些血液瘤中,bispecific antibodies 的即用性、成本與可及性正在挑戰 CAR-T。未來 CAR-T 必須證明自己在深度緩解與長期疾病控制上有無可取代的地位。
這才是 CAR-T 的下一個十年。不是每個 CD19 CAR-T 都值得投。不是數據漂亮就能出大藥廠BD的。不是每條漂亮早期數據都能變成百億市場。
【結語|強生砍掉的不是希望,而是幻想】
✨ Johnson & Johnson 這次停掉 JNJ-9530 與 JNJ-4496,表面上是一場管線調整,實際上是整個 CAR-T 產業進入成熟期後的一次現實教育。它告訴我們三件事。
- 第一,漂亮早期數據不等於商業成功。
- 第二,自體 CAR-T 的成本、製造與給付問題,會吞掉很多看似美麗的臨床故事。
- 第三,沒有壓倒性差異化的自體 CD19/CD20 CAR-T,BD 大藥廠預期應該被大幅重估。
自體 CD19 CAR-T 如果只是跟著全球已成熟標靶做 me-too,很難再有 BD 大藥廠想像。這條賽道不是沒有科學價值,而是大型買家已經不缺這種資產。真正值錢的,是能改變成本結構、治療場景、製造流程和疾病定位的下一代技術。嬌生這次不是宣告 CAR-T 終結。
它宣告的是:自體 CD19 CAR-T 靠早期反應率講故事的時代結束了。
接下來的 CAR-T 競爭,不再是誰的故事更熱血。而是誰能在療效、安全性、製造、給付和商業化之間,真正跑出一個能活下來的模型。
-----------
參考資料:
[0]: 各公司官網&公開資料
[1]: https://www.jnj.com/media-center/press-releases/johnson-johnson-statement-on-investigational-programs-in-large-b-cell-lymphoma
[2]: https://www.jnj.com/media-center/press-releases/johnson-johnsons-dual-targeting-car-t-cell-therapy-shows-encouraging-first-results-in-large-b-cell-lymphoma
[3]: https://www.fda.gov/drugs/resources-information-approved-drugs/fda-approves-axicabtagene-ciloleucel-second-line-treatment-large-b-cell-lymphoma
[4]: https://www.gileadclinicaltrials.com/study
[5]: https://www.investor.jnj.com/investor-news/news-details/2026/Johnson--Johnson-reports-Q1-2026-results-raises-2026-outlook/default.aspx

















