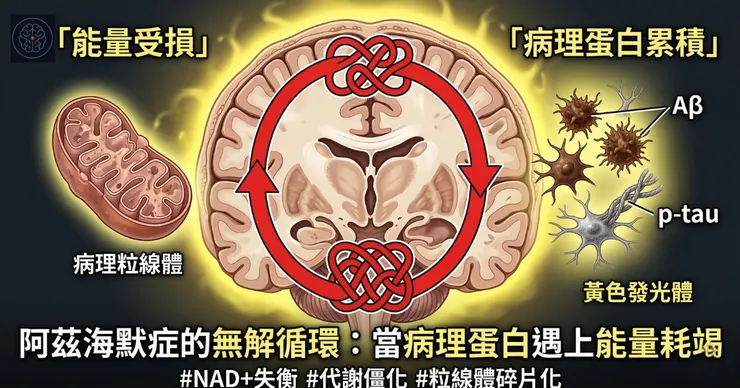
阿茲海默症病理機制
說到阿茲海默症(Alzheimer's Disease, AD),大多數人第一時間聯想到的可能是大腦中堆積的「類澱粉蛋白」與「tau 蛋白」。然而,近年來科學家發現,這其實更像是一場大腦神經元的「能源危機」!
阿茲海默症與我們細胞內的發電廠——「粒線體(Mitochondria)」,有著高度的雙向因果關係。當粒線體能量受損,不僅會引發分子層面的代謝破壞,還會導致細胞清理機制失效,甚至剝奪整個大腦網絡的能量。今天,就讓我們透過 6 個關鍵機制,深入了解阿茲海默症背後的「大腦能量崩潰」真相:
1. 發電廠核心停擺:克氏循環遭破壞與 ATP 產量中斷
大腦運作需要極高的能量,而這些能量(ATP)主要由粒線體內的「克氏循環(檸檬酸循環)」來製造。研究發現,在阿茲海默症患者腦中,神經元的代謝相關酵素會發生一種異常的**「硫基亞硝基化(S-nitrosylation)」反應**。 在這種異常反應中,氮和氧原子被異常標記成硫原子,直接導致克氏循環中製造「琥珀酸(succinate)」的步驟出現問題。由於琥珀酸是驅動後續能量分子 ATP 生產的關鍵要素,這項異常會讓粒線體無法產出足夠的能量,神經元及其突觸連接自然就失去了維繫的動力。
2. 細胞修復小幫手缺貨:關鍵輔酶 NAD+ 嚴重失衡
NAD+ 是細胞產生能量、維持運作與氧化磷酸化過程中不可或缺的輔酶。隨著年齡增長,體內的 NAD+ 本來就會逐漸減少,但在阿茲海默症的病理狀態下,大腦內 NAD+ 會出現更嚴重的失衡與消耗。這不但會影響粒線體的能量代謝,還會大幅削弱神經細胞在面對氧化壓力與發炎時的自我修復能力。
3. 發電廠過度碎裂:粒線體動態失衡
健康的粒線體必須透過不斷的「融合(fusion)」與「分裂(fission)」來維持形狀與代謝穩定。但在阿茲海默症中,這項動態平衡遭到嚴重破壞。患者腦中促使分裂的蛋白質(如 Fis1、Drp1)異常增加,而促進融合的蛋白質(如 Mfn1/2、OPA1)減少。這導致粒線體過度碎片化,無法有效傳輸到神經突觸,最終引發嚴重的神經突觸功能障礙與退化。
4. 細胞清潔系統當機:粒線體自噬(Mitophagy)功能缺陷
正常情況下,細胞有一套名為「粒線體自噬」的回收機制,能清除受損或老化的粒線體,維持細胞健康。這套系統高度仰賴 PINK1 和 Parkin 等關鍵蛋白質的調控。但在阿茲海默症大腦中,PINK1 和 Parkin 的濃度顯著下降,導致自噬作用減弱。這使得失去產能作用的「廢棄粒線體」在神經元內大量堆積,進一步引發細胞內鈣離子失衡與嚴重的氧化壓力。
5. 搶糧大戰:大腦細胞的「代謝僵化」與神經元能量剝奪
阿茲海默症大腦會出現一種稱為**「代謝僵化(Metabolic inflexibility)」的現象。為了應對病理環境與神經發炎,大腦的支援部隊——微膠質細胞(Microglia)和星形膠質細胞,會將代謝模式從高效的粒線體氧化磷酸化,轉向產能效率極低的「糖解作用(Glycolysis)」。 這些膠質細胞為了維持發炎反應,開始壟斷大腦中的葡萄糖資源,打破了原本星形膠質細胞供應乳酸給神經元產能的合作機制(ANLS)。這種惡性競爭直接剝奪了神經元的能量來源,導致神經元因缺乏 ATP 而喪失傳遞訊號的能力**。
6. 走向深淵:能量受損與病理蛋白的「惡性循環」
最可怕的是,上述的能量缺乏與氧化壓力,會加劇阿茲海默症的核心病理特徵:類澱粉蛋白的累積與 tau 蛋白的過度磷酸化。反過來,這些累積的有毒類澱粉蛋白與 p-tau 會直接攻擊粒線體;例如,p-tau 會與 Drp1 相互作用並增強其活性,引發更嚴重的粒線體碎裂與功能障礙。這兩者形成了一個互相拖累的「惡性循環」,促使疾病持續惡化。
💡 科學帶來的新希望:逆轉能量危機! 雖然阿茲海默症的病理機制錯綜複雜,但這項關於「能量受損」的發現也為治療帶來了全新曙光。近期的動物實驗顯示,如果能透過實驗藥物(如 P7C3-A20 或 NAD+ 前驅物)來恢復腦內 NAD+ 的能量平衡,即使在疾病已經進展的情況下,小鼠的記憶與認知表現仍能出現明顯的回升。另外,科學家也發現透過補充特定的小分子類似物來重啟停滯的克氏循環,能有效修復損毀的神經突觸。
保養大腦,除了持續學習與運動,或許未來我們能透過「恢復大腦能量代謝」的療法,真正逆轉阿茲海默症!
(想了解更多關於大腦健康與醫學新知,歡迎訂閱我們的部落格或在下方留言分享你的看法!)
























