YT: https://youtu.be/Dom5fw1t3kI
法說PDF: https://mopsov.twse.com.tw/nas/STR/678520260420M001.pdf
法說影音: http://irconference.twse.com.tw/6785_10_20260420_ch.MP4
昱展新藥(6785)ALA-3000臨床一期展現優異療效與安全性,成功克服Ketamine副作用。公司以長效藥物平台為核心,布局憂鬱症、帕金森與思覺失調症,並拓展至胜肽領域,具備長期成長潛力。
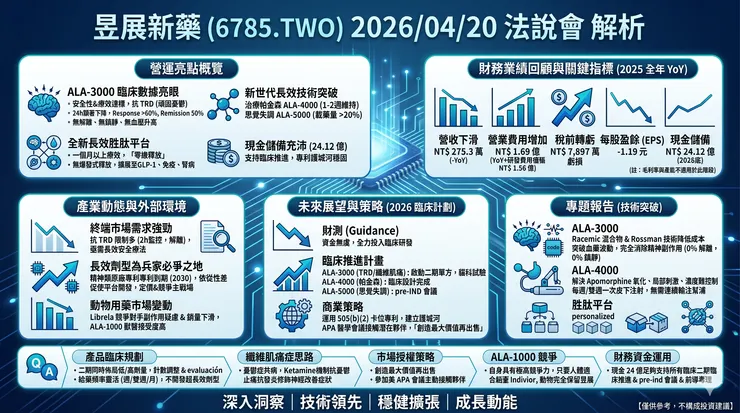
1. 營運亮點概覽 (Executive Summary)
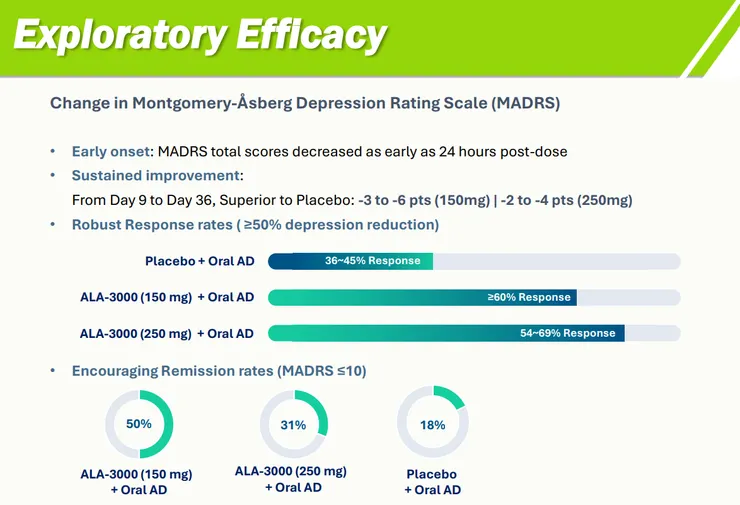
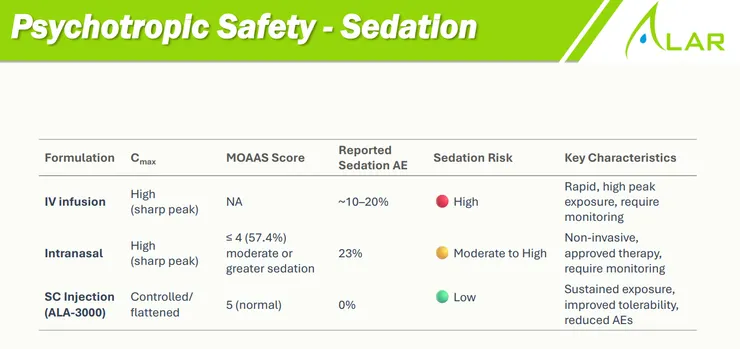
- ALA-3000 臨床一期數據亮眼,安全性與療效雙雙達標:針對頑固型憂鬱症 (TRD) 的長效 Ketamine 皮下注射劑 ALA-3000,一期臨床顯示給藥後 24 小時憂鬱分數即顯著下降,且 Response rate (反應率) 大於 60%、Remission rate (緩解率) 達 50%,顯著優於安慰劑組。安全性方面,成功克服傳統 Ketamine 痛點,無解離 (Dissociation)、無鎮靜 (Sedation)、無血壓升高及泌尿毒性。
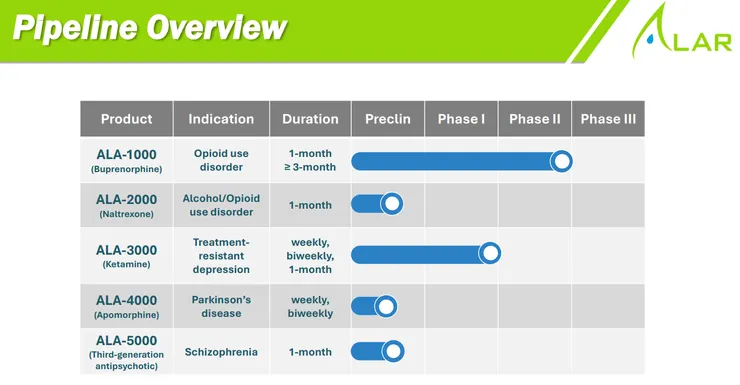
- 新世代長效技術突破,打造強大產品線 (Pipeline):除了 ALA-3000,治療帕金森氏症的 ALA-4000 (長效 Apomorphine) 單針可維持 1-2 週療效,有望取代現有連續輸注幫浦。思覺失調症口服長效藥物 ALA-5000 突破溶解度瓶頸,載藥量達 20% 以上,預計明年進入臨床。
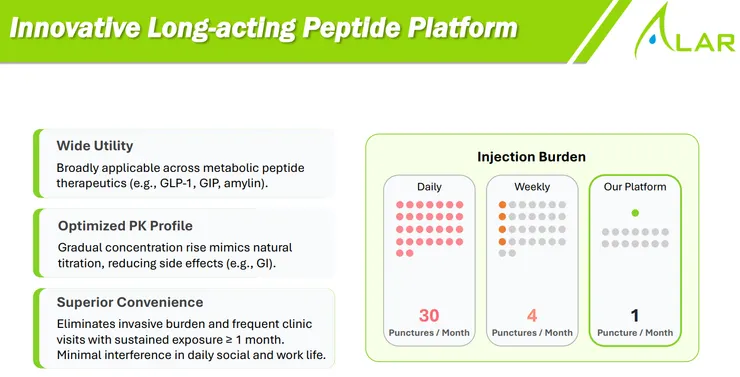
- 全新長效胜肽平台 (Peptide Platform) 開啟新成長曲線:動物試驗證實單針注射可維持一個月以上療效,且具備「零級釋放 (Zero-Order Release)」特性,無爆發式釋放 (Burst release),未來將擴展至 GLP-1 等代謝藥物、免疫與腎病領域,跨出中樞神經 (CNS) 限制。
- 現金儲備極度充沛,專利護城河穩固:截至 2025 年底帳上現金達新台幣 24.12 億元,足以支撐旗下多項核心藥物推進一、二期臨床試驗。PCT 專利審查取得重大突破,24 項專利請求項 (Claims) 針對新穎性、進步性及工業可行性全數獲准。
2. 財務業績回顧與關鍵指標 (Financials & Key Metrics)
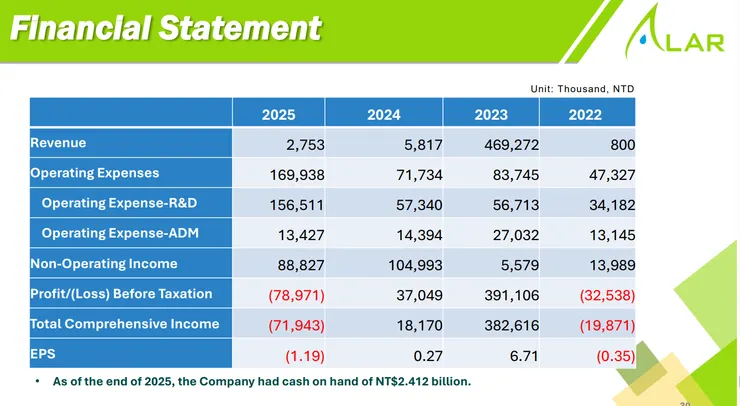
- 營收與獲利表現 (QoQ / YoY): 2025 年全年營收為新台幣 275.3 萬元,較 2024 年的 581.7 萬元與 2023 年的 4.69 億元顯著下降。 2025 年營業費用為新台幣 1.69 億元,相較 2024 年的 7,173 萬元大幅增加,主要因研發費用擴張(2025 年研發費用達 1.56 億元)。 2025 年稅前虧損為新台幣 7,897 萬元,較 2024 年稅前盈餘 3,704 萬元轉虧。
- 關鍵財務比率: 每股盈餘 (EPS):2025 年 EPS 為 -1.19 元(2024 年為 0.27 元)。 (註:作為研發型生技公司,毛利率與產能利用率等傳統製造業指標不適用於此階段)。
- 資本與營運效率: 充沛的現金流:截至 2025 年底,公司帳上現金高達新台幣 24.12 億元,為未來兩年推進各項臨床試驗提供強而有力的資金後盾。
3. 產業動態與外部環境 (Industry & Macro Environment)
- 終端市場需求強勁:針對 TRD (頑固型憂鬱症) 領域,現有治療選項如 Spravato (J&J) 存在需要 2 小時臨床監控、不可駕車等嚴格限制,且會產生解離等副作用,對醫療機構及病患造成巨大負擔。市場亟需能消除這些限制的長效且安全的替代療法。

- 長效劑型為未來十年兵家必爭之地:原廠精神類藥物專利預計將於 2030 年陸續到期,全球藥廠正積極推動長效平台以解決口服藥物依從性差的限制,長效產品將成為未來定價與競爭的主戰場。
- 總體政策利多:美國政府近期簽署法案鼓勵迷幻藥研發,特別是針對退伍軍人的醫療需求並提供補助,對相關創新療法上市具備政策推力,惟 FDA 審核標準依然嚴格。
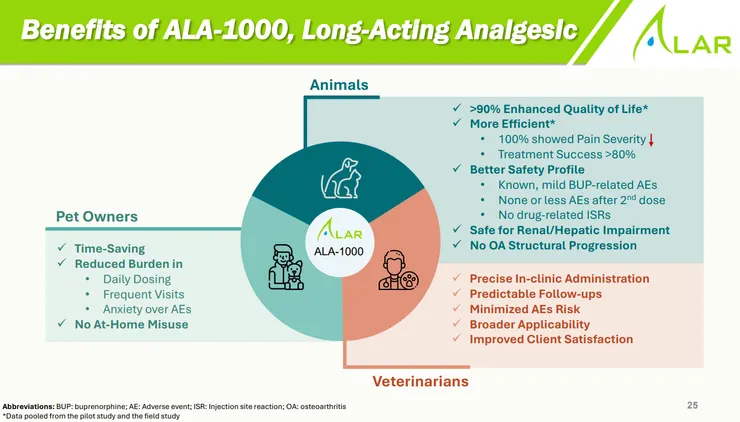
- 動物用藥市場變動:獸醫 OA 疼痛市場中,競爭對手 Librela (單株抗體) 因副作用疑慮引發飼主訴訟與銷量下滑,為昱展小分子長效藥物 ALA-1000 創造了切入點,獸醫師對 ALA-1000 的接受度與信心極高。
4. 未來展望與策略 (Guidance & Strategy)
- 財測 (Guidance):公司未提供具體的次季或全年營收財測數字,但明確表示目前資金無虞,將全力投入臨床研發。
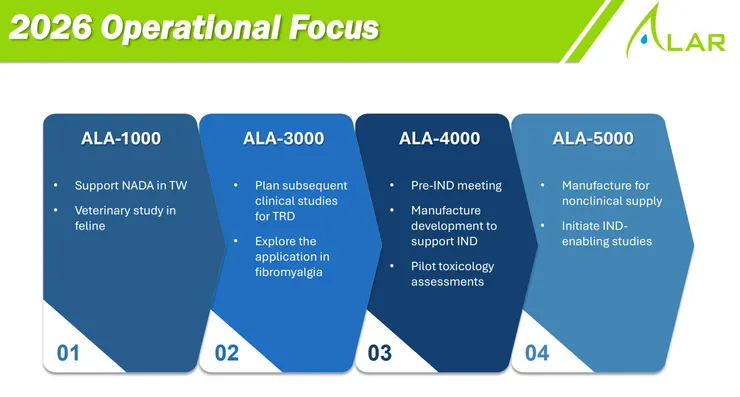
- 中長期營運目標與臨床推進計畫: ALA-3000 (TRD/纖維肌痛症):2026 年預計啟動二期單方臨床試驗,並拓展極具潛力的「纖維肌痛症」新適應症。同時準備支持台灣動物用藥 (NADA) 藥證與貓科試驗。 ALA-4000 (帕金森氏症):2026 年計畫完成後續針對 TRD (簡報列為 TRD,可能為筆誤或指探索階段) 的臨床設計,並探索纖維肌痛症應用。 ALA-5000 (思覺失調症):2026 年預計進行 Pre-IND 會議、IND 授權製造開發與前導毒理評估。 ALA-1000 (OUD):推動非臨床製造供應及 IND 授權試驗。
- 商業與授權策略:運用 505(b)(2) 途徑卡位長效技術專利,建立強大護城河。公司預計於 5 月參與美國 APA 醫學會議,主動接觸具備長效產品營銷經驗的潛在夥伴,並堅持「創造最大價值再出售」的談判策略。
5. 專題報告 (Special Topics)
- ALA-3000 (長效 Ketamine 皮下注射劑): 技術突破:運用 Racemic 混合物與 Rossman 技術降低成本,突破了靜脈注射或鼻噴劑型血藥濃度劇烈波動的缺點,實現了數週的穩定釋放。 臨床表現:一期臨床完全消除了「峰值驅動 (Peak-driven)」的精神副作用 (0% 解離風險、0% 鎮靜風險)。
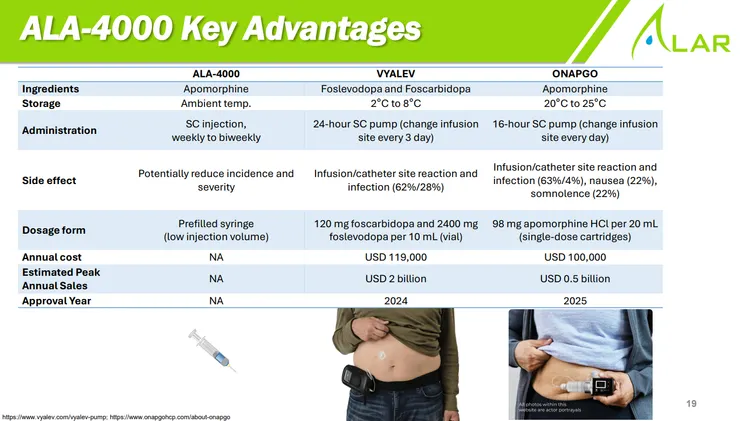
- ALA-4000 (長效 Apomorphine 皮下注射劑): 技術突破:解決了 Apomorphine 分子極易氧化、具局部刺激性且濃度難以控制的歷史難題。 產品優勢:無需依賴昂貴且操作複雜的 24 小時連續輸注幫浦,只需每週/雙週一次皮下注射,大幅減輕帕金森氏症患者與照護者的負擔。
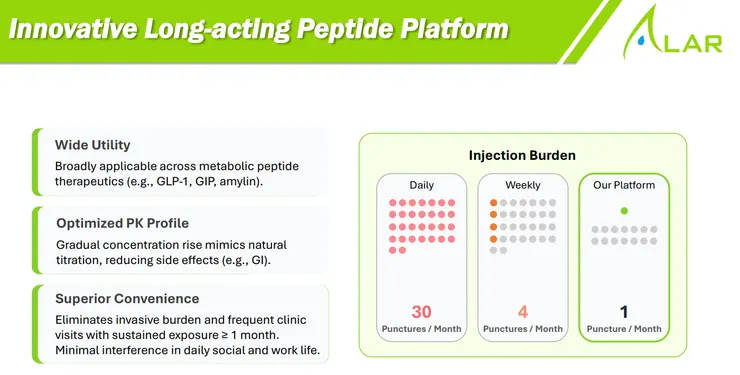
- 新事業板塊:創新長效胜肽平台 (Innovative Long-acting Peptide Platform): 技術亮點:這是一個全新的長效平台,單次注射療效可達一個月以上。其最大優勢在於「零級釋放 (無爆發式釋放)」,濃度上升平緩,能有效避免傳統 GLP-1 (如 Semaglutide) 因濃度劇烈波動而導致的腸胃道副作用或補償性進食。 應用潛力:將可廣泛應用於 GLP-1、GIP、amylin,甚至免疫與腎病領域,開啟公司跨出 CNS 的全新成長動能。
6. 潛在風險與挑戰 (Risks & Challenges)
- 法規與監管風險:Ketamine 屬三級管制藥品,美國 FDA 針對其濫用風險與精神副作用設有嚴格的 REMS 規範(如 2 小時留院監控)。雖然 ALA-3000 旨在消除這些限制,但仍需與 FDA 進行深度溝通以取得法規上的鬆綁認可。
- 開發與審查時程延遲風險:管理層主動提及,ALA-1000 此前因授權夥伴 Indivior 需評估放大及三期製程的穩定性問題,導致計畫有所延遲,顯示外部夥伴的進度控管可能成為營運變數。
- 定價與商業保險涵蓋風險:長效製劑若開發為 2 至 3 個月的超長效產品,單價勢必大幅提高,可能面臨商業保險公司嚴格的審查與給付阻力,因此公司目前將療程策略性控制在 1 個月以內。
- 臨床試驗的破盲風險:傳統迷幻藥療法因受試者容易察覺解離副作用,導致臨床試驗容易「破盲 (Unblinding)」,引發 FDA 疑慮;所幸 ALA-3000 無解離現象,可大幅降低此風險。
7. 問答環節精華 (Q&A Highlights)
【產品技術與臨床規劃類】
- Q: ALA-3000 有低劑量和高劑量,針對臨床二期會怎麼樣規劃?
- A: 二期臨床將同時佈局低、高劑量組,並針對高劑量組可能調整(降低)注射體積以減少局部反應,同時增加註射針數並擴大樣本量以進行更長期的評估。給藥頻率將具靈活性(如一週、兩週或一個月),基於醫療保險給付與診所管理的現實需求,目前不考慮開發兩至三個月的超長效劑型,一個月一針已足夠。
- Q: 關於新增纖維肌痛症的思路是?
- A: 纖維肌痛症患者常與憂鬱症共病。動物實驗顯示症狀有明顯改善,且 Ketamine 的機制本身就對抗憂鬱、止痛、抗發炎有效,能透過長期修飾神經發炎改善症狀,是一項潛力極大的全新適應症。
【市場授權與商業策略類】
- Q: 請問 ALA-3000 現在臨床下一階段的設計,是否在授權過程中遇到不如預期的狀況,需要額外數據?
- A: 目前尚未正式開始談判,預計五月參加美國 APA 會議時主動接觸相關對象。授權策略會創造最大價值再出售,若單一療法能驗證療效,意義將非常重大。
- Q: 關於 ALA-1000 的問題,授權夥伴是否有壓力要刪減產品?還是先推現有產品,然後 ALA-1000 就放著?
- A: 無法替對方判斷或解讀,但公司認為自身的產品具有極高的競爭力。
- Q: 我們授權的 ALA-1000 是否只限於壓力相關適應症?還是所有人體適應症都包含在合約範圍?
- A: 只要是人體適應症,都授權給 Indivior,合約涵蓋所有人體適應症;但動物用藥的權利仍完全由昱展保留與主導。
【財務與資金運用類】
- Q: 是否因現金越來越充裕,會將部分有把握的藥物推進到二期臨床?
- A: 截至去年底帳上現金約 24 億元,資金非常充裕,絕對足夠支持 ALA-3000 進入二期臨床,以及 ALA-4000 和 ALA-5000 進入一期臨床,無資金匱乏之虞。
免責聲明 (Disclaimer)
本文章/資料之內容僅供參考,不構成任何形式之投資建議、要約、招攬或勸誘。
文中所述之財務數據、營運狀況、預測及產業展望,皆基於公司法說會之口述內容或特定時間點之公開資訊整理而成。未來實際發展可能因總體經濟、產業環境、市場競爭等各種客觀因素變動,而與本文內容或預期有所差異。
本資料可能包含由人工智慧(AI)輔助生成或轉錄之內容,雖已力求語意通順與資訊客觀,但無法保證其完整性與絕對正確性,亦可能存在解讀上的誤差,所有數據與營運資訊應以該公司於「公開資訊觀測站」發布之正式公告為準。
投資一定有風險,金融市場具備波動性。閱聽人及投資者於進行任何投資決策前,應自行獨立判斷、審慎評估相關風險,並自負盈虧。對於任何因直接或間接使用本文資訊而造成之財務損失,本文作者、發布平台及相關資訊提供者概不負責。